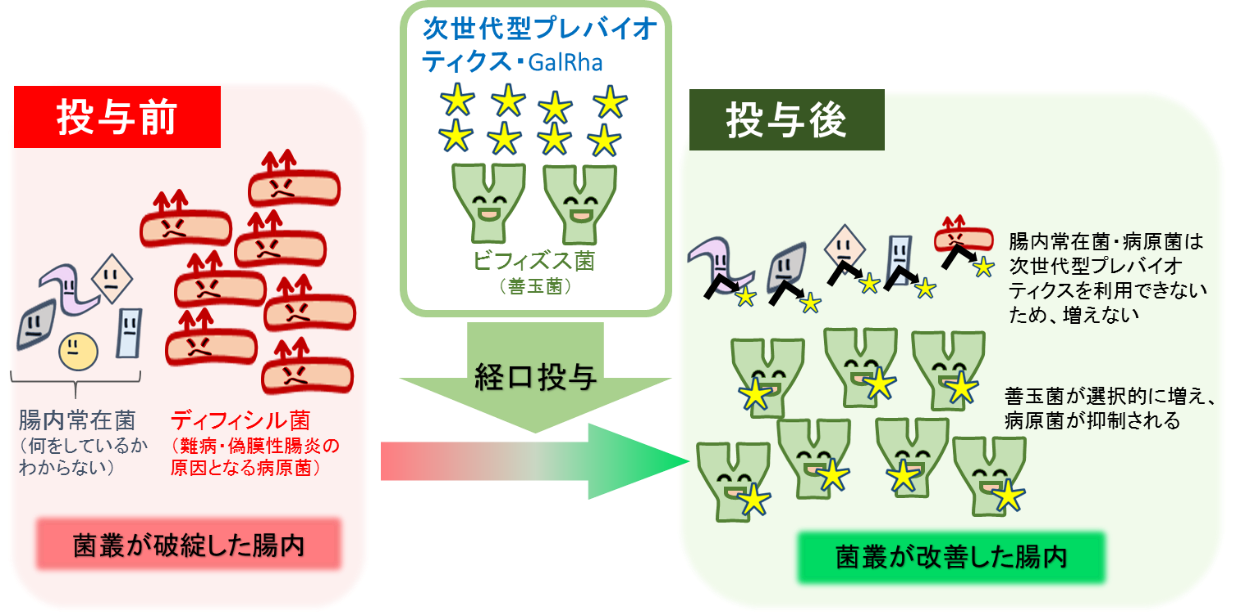
善玉菌のみを増殖させる次世代型プレバイオティクス※1 を発見 難病である偽膜性腸炎の新たな治療法開発に期待

近畿大学生物理工学部(和歌山県紀の川市)食品安全工学科 准教授 栗原 新、新潟大学農学部(新潟県新潟市)農学科 食品科学プログラム 准教授 中井 博之、石川県立大学大学院(石川県野々市市)博士後期課程3年 平野 里佳を中心とする研究グループは、ビフィズス菌を選択的に増殖させることのできる「次世代型プレバイオティクス」となりうるオリゴ糖を発見しました。「プレバイオティクス」とは、善玉菌を増殖させ腸内環境を改善する物質で、特に今回発見した特定のオリゴ糖とビフィズス菌の組み合わせは、偽膜性腸炎※2 の新たな治療法開発につながる可能性を示しました。
本件に関する論文が、令和3年(2021年)9月23日(木・祝)21:00(日本時間)に、イギリスのTaylor & Francis社発行の腸内細菌や微生物に関する学術雑誌“Gut Microbes”に掲載されました。
【本件のポイント】
●ビフィズス菌などの善玉菌だけを選択的に増殖させるオリゴ糖(ガラクトシル-β1,4-ラムノース)を発見
●ビフィズス菌が特定のオリゴ糖を栄養源として生育する際に必要な遺伝子を特定
●特定のオリゴ糖とビフィズス菌を組み合わせて経口摂取することで、偽膜性腸炎の原因菌の生育を抑制
【本件の背景】
プレバイオティクスは、腸内環境を改善する目的でサプリメントや食品添加物として経口摂取されますが、大腸まで到達する必要があるため、「ヒトには消化されない」という性質を持つ難消化性糖質※3 が用いられます。しかし、大腸に到達したプレバイオティクスは腸内に常在する様々な細菌に利用されるため、腸内常在細菌に「横取り」された場合、目的の善玉菌に行きわたらない可能性があります。今回の研究の過程でも、既存のプレバイオティクスの多くが様々な腸内常在細菌に利用される可能性が明らかになっています。さらに、近年の腸内細菌学の進展により、様々な腸内常在細菌がヒトに悪影響を与えていることも明らかになっているため(Cell, 2016, 165:842-853; Cell, 2016, 167:1339-1353.)、プレバイオティクスを開発する際は、悪い働きをする腸内常在細菌が増殖しないよう気を配る必要があります。
以上の課題を解決する目的で、特定の善玉菌だけを増やすことができる「次世代型プレバイオティクス」の開発を目指して研究を行いました。
【本件の内容】
研究チームはまず、ヒト腸内常在菌叢※4 のうち菌数の多い27菌種(Nature, 2010, 464:59−65.)およびビフィズス菌・乳酸菌・病原菌を試験管内で培養し、このうちビフィズス菌だけを選択的に増殖させる「ガラクトシル-β1,4-ラムノース(以下、GalRha)」というオリゴ糖を、11種類のガラクトオリゴ糖の中からのスクリーニング※5 により発見しました。また、ビフィズス菌を、偽膜性腸炎の原因菌であるディフィシル菌と共にGalRhaを含む培地で培養すると、ディフィシル菌の増殖が抑制されることを明らかにしました。
さらに、ヒトへの応用を視野に入れ、ヒト糞便、ビフィズス菌、ディフィシル菌を同時に培養したところ、GalRhaを含む培地では、含まない培地と比較してディフィシル菌の毒素産生が大きく抑制されました。本研究成果によって、GalRhaとビフィズス菌を組み合わせることによって、難病として知られる偽膜性腸炎の新たな治療法開発につながる可能性が示されました。

【論文掲載】
掲載誌:Gut Microbes(インパクトファクター:10.245@2020)
論文名:
Next-generation prebiotic promotes selective growth of bifidobacteria, suppressing Clostridioides difficile
(ビフィズス菌を特異的に増殖させる次世代型プレバイオティクス・ガラクトシル-β-1,4-ラムノースは、Clostridioides difficileの増殖を抑制する)
著 者:
平野 里佳1,2、阪中 幹祥1、吉見 一人3,4、杉本 直久5、江口 省吾5、山内 祐子3,4、奈良 未沙希1、前田 信悟1、網 優太2、後藤 愛那6、片山 高嶺1,6、飯田 宗穂7、加藤 完8、大野 博司8、吹谷 智9、横田 篤9、西本 完10、北岡 本光5,10、中井 博之5※ 、栗原 新1,2※
※ 共同責任著者
所 属:
1 石川県立大学大学院生物資源環境学研究科、2 近畿大学生物理工学部、3 東京大学医科学研究所、4 大阪大学医学部、5 新潟大学農学部、6 京都大学大学院生命科学研究科、7 金沢大学附属病院、8 理化学研究所生命医科学研究センター、9 北海道大学大学院農学研究院、10 農研機構・食品研
【研究の詳細】
研究チームは、「次世代型プレバイオティクス」を探し出すため、ヒト腸内常在菌叢のうち優勢な27菌種およびビフィズス菌・乳酸菌・病原菌を、GalRhaを添加した培地と添加していない培地で培養し、生育度を比較しました。その結果、腸内常在菌叢優勢種や病原菌はほとんど増殖が促進されず、乳酸菌やビフィズス菌といった善玉菌は増殖が大きく促進されました。
次に、GalRhaのみを炭素源として添加した培地で、ビフィズス菌野生株とビフィズス菌BL105A_0502変異株(BL105A_0502を働かなくした株)を培養したところ、ビフィズス菌BL105A_0502変異株の生育が大幅に遅れたことから、基質結合タンパク質BL105A_0502がビフィズス菌のGalRhaの利用に必要であることが示されました。
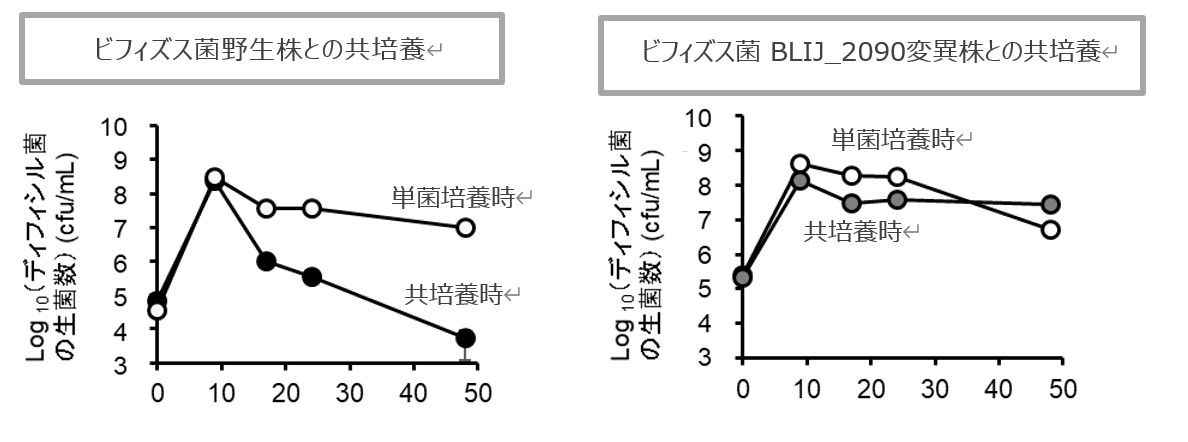
また、GalRhaを含む培地でビフィズス菌とディフィシル菌を共培養し、単菌培養時のディフィシル菌の生菌数(下左図:白)と比較したところ、ビフィズス菌野生株との共培養時のディフィシル菌の生菌数(下左図:黒)は大幅に減少しました。これに対して、ビフィズス菌 BLIJ_2090(BL105A_0502のホモログ※6 )変異株との共培養のディフィシル菌の生菌数(下右図:灰)は、単菌培養時のディフィシル菌の生菌数(下右図:白)と比較して差が見られませんでした。

さらに、ヒトへの応用を視野に入れ、GalRhaを含む培地でヒト糞便由来細菌、ビフィズス菌、ディフィシル菌を同時に培養すると、ディフィシル毒素産生量はGalRhaを添加してビフィズス菌と共に培養することで大幅に減少しました。
また、マウスにディフィシル菌を感染させると経日的に体重が減少し、その後の回復は見られませんでしたが、ディフィシル菌感染1日目、3日目、5日目にビフィズス菌とGalRhaを同時投与した場合は、5日目にかけて経日的な体重減少が見られたものの、7日目にはディフィシル菌感染前レベルにまで体重が回復しました。
これらの結果から、GalRhaとビフィズス菌を組み合わせることによって、偽膜性腸炎の原因となるディフィシル菌の生育が抑制されることが明らかになりました。本研究成果によって、難病として知られる偽膜性腸炎の新たな治療法開発につながる可能性が示されたと言えます。
【今後の展望】
本研究成果は、GalRhaを治療に応用するための第一歩です。今後、投与量や投与方法を工夫し、ヒトの臨床試験を行うことで、次世代型プレバイオティクスを活用した偽膜性腸炎の新たな治療法を開発できる可能性があります。
同様の手法を用いることで、ビフィズス菌のみならず、乳酸菌、酪酸菌、アッカーマンシア菌などの善玉菌を選択的に増殖させる技術を開発することもできます。また、2型糖尿病(Nature, 2012, 490:55-60.)、クローン病(J. Gastroenterol. Hepatol. 2013, 28:613-619.)、1型糖尿病(ISME J. 2011, 5:82-91.)、肥満(Science, 2013, 341:1231214.)で特徴的に減少している腸内細菌を選択的に増殖させることで、これらの疾患を治療できる次世代型プレバイオティクスを開発できる可能性があります。
さらに、個人差の大きい腸内細菌叢に対応し、1人ひとりに最適なオリゴ糖を選択することで、オーダーメイドプレバイオティクス※7 の開発にも期待ができます。
【用語解説】
※1 プレバイオティクス:宿主(ヒトや動物)に常在する微生物が選択的に利用することで、宿主に健康上のメリットをもたらす物質(Nature Reviews Gastroenterology & Hepatology 2017; 14:491-502.)。
※2 偽膜性腸炎:腸粘膜に偽膜形成をみる抗菌薬起因性腸炎。原因は抗菌薬投与により腸内細菌叢が変化し増殖するClostridioides difficile(ディフィシル菌)などの菌毒素である(日本救急医学会・医学用語解説集)。
※3 難消化性糖質:ヒトの消化酵素で分解されず大腸まで届くと考えられている糖質。
※4 ヒト腸内常在菌叢:ヒトの腸内に常在する多種多様な細菌が混合された共同体。
※5 スクリーニング:多くの種類の物質の中から目的の性質を持つ物質を選び出すこと。
※6 ホモログ:あるタンパクとアミノ酸配列がよく似たタンパク(あるいはある遺伝子と塩基配列がよく似た遺伝子)。
※7 オーダーメイドプレバイオティクス:個人差の大きいヒトの腸内細菌叢に合わせた、個人毎に異なるプレバイオティクス。
【関連リンク】
生物理工学部 食品安全工学科 准教授 栗原 新(クリハラ シン)
https://www.kindai.ac.jp/meikan/2313-kurihara-shin.html