マルチオミクス解析によりミトコンドリア病未解決症例の原因を特定 ~遺伝性疾患の診断におけるマルチオミクス解析の重要性~
【概要】
近畿大学理工学部生命科学科講師の木下 善仁(順天堂大学 難病の診断と治療研究センター 非常勤講師)と順天堂大学難病の診断と治療研究センターの岡﨑 康司 教授、千葉県こども病院の村山 圭 部長、および埼玉医科大学小児科 大竹 明 教授らの共同研究により、遺伝子診断で未診断となっていたミトコンドリア病※1 症例のマルチオミクス解析※2 を行い、NDUFV2遺伝子の変異を同定し原因を特定しました。RNAシーケンス※3 や全ゲノム解析※4 を行うことによって、従来の遺伝子診断法の全エクソーム解析※5 では見出すことができなかった遺伝子欠失をはじめて明らかにしました。本成果により、遺伝性疾患の診断においてマルチオミクス解析を導入することの重要性が示されました。本論文はHuman Mutation誌のオンライン版に2021年9月2日付で公開されました。
【本研究成果のポイント】
●従来解析で未解決となっていたミトコンドリア病症例の原因をマルチオミクス解析により特定
●Alu因子※6 を介した非常に珍しい遺伝子欠失を同定
●遺伝性疾患の診断におけるマルチオミクス解析の重要性が示された
【背景】
ミトコンドリアの機能異常が原因となる病気を総称してミトコンドリア病と呼んでいます。この疾患の発症年齢や症状、遺伝形式は多岐に渡っており、臨床的また遺伝的に診断が非常に難しい疾患です。
岡﨑教授らの研究グループは十数年にわたり、千葉県こども病院代謝科(村山 圭 部長)、埼玉医科大学小児科(大竹 明 教授)と共同で、ミトコンドリア病の生化学診断や遺伝子診断に取り組んできました。この疾患の診断は非常に難しく、その診断率はおよそ30-40%となっています。遺伝子診断ではこれまで全エクソーム解析などを中心として行われてきましたが、遺伝子のエクソン領域を対象にした解析のため、技術的な限界があることが課題でした。これらの問題を解決するため、研究グループはRNAシーケンスや全ゲノム解析等を組合わせたマルチオミクス解析を駆使し、原因解明に取り組みました。
【内容】
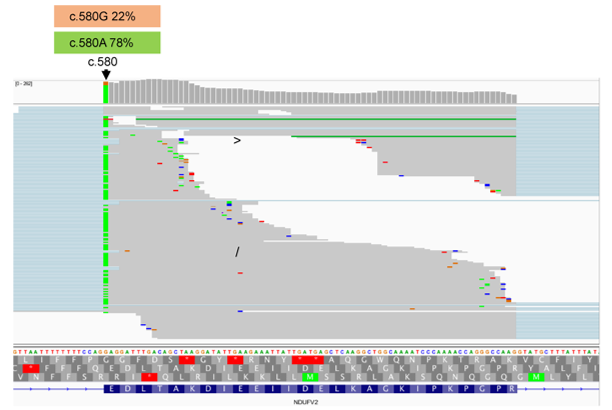
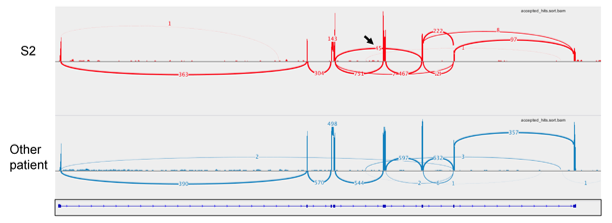
今回、ミトコンドリア病の未解決症例を対象として、マルチオミクス解析を行いました。対象となる症例はミトコンドリア呼吸鎖Iの異常を呈しており、生化学診断によりミトコンドリア病とされていました。従来のゲノム解析方法である全エクソーム解析を用いて原因探索を行い、NDUFV2遺伝子にヘテロ接合のc.580G>A(p.Glu194Lys)の遺伝子異常を有することを見い出しました。この遺伝子異常は、ヘテロ接合の状態では病的原因と考えられないため、さらなる遺伝子異常が存在することが示唆されました。そこで、RNAシーケンス(RNA-seq)と全ゲノム解析を実施し、遺伝子異常の探索を行いました。その結果、RNAシーケンスのデータから遺伝子発現の偏り(図1)があること、およびエクソンスキップが起こっていることを発見しました(図2)。


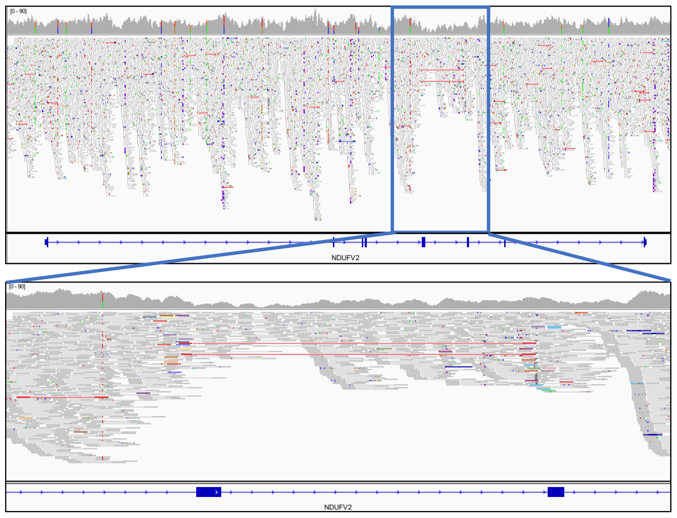
全ゲノム解析を行った結果では、NDUFV2遺伝子のイントロン4-エクソン5-イントロン5にまたがる遺伝子欠失が存在することがわかりました(図3)。RNAシーケンスでエクソンスキップしていたエクソン5を巻き込んだ欠失であったことから、これが疾患の原因と考えられました。

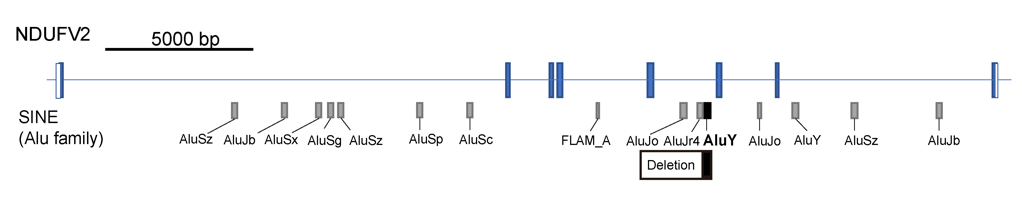
次に、PCRとサンガーシーケンス※7 により欠失の詳細を調べました。その結果、この欠失はAlu因子を介した欠失であることが分かりました。Alu因子はゲノム上を移動するトランスポゾンであり、今回の場合はAlu因子がゲノム上を移動した結果、周辺の領域を巻き込んだ欠失を起こしていたことが示唆されました(図4)。このような現象は稀であり、典型的なミトコンドリア病としては初めて示された症例です。タンパク質の発現量の解析では、NDUFV2タンパク質が顕著に発現低下していることがわかりました。NDUFV2はミトコンドリア呼吸鎖複合体Iの構成成分で、鉄硫黄クラスターを介し電子伝達系に重要な働きをもつことが知られており、この機能異常が患者における神経筋症状の発症につながったと考えられます。
以上より、ミトコンドリア病の未解決症例においてマルチオミクス解析により疾患原因となるNDUFV2遺伝子異常を特定することができました。

【今後の展開】
本成果において、未解決となっていたミトコンドリア病に対してマルチオミクス解析を行うことで最終的な遺伝子診断を下すことができました。今回の結果から、遺伝子診断のためにマルチオミクスを導入することの重要性が示されました。他の疾患においても、このようなマルチオミクス解析の応用が可能であり、将来的に遺伝子診断にこの技術が普及することが期待されます、本研究結果は、その成功例としてマルチオミクス解析の重要性を示しました。また、非常に稀なAlu因子を介した遺伝子欠失を見出したことから、今後も関連疾患の中にこのような遺伝子異常が発見されることも予想されます。また、NDUFV2遺伝子異常を持つ症例の線維芽細胞に対して、アミノレブリン酸とクエン酸第一鉄ナトリウムの投与が有効であることが当研究グループの先行研究で示されてることから、治療薬としての可能性が考えられます。今後遺伝子異常と治療薬の適応についての研究が進むことが期待されます。
【用語解説】
※1 ミトコンドリア病
ミトコンドリア病とは、ミトコンドリアの働きが低下することが原因で起こる病気の総称です。国の指定難病および小児慢性特定疾病に定められています。いかなる症状、いかなる臓器・組織、何歳でも、いかなる遺伝形式でも発病するとされています。
※2 マルチオミクス解析
マルチオミクスとはMulti(多数の)とOmics(オミクス)を組み合わせた造語であり、オミクスとは生体分子を網羅的に解析することを意味しています。オミクスはDNA、RNA、タンパク質、代謝物などが対象となり、それぞれゲノミクス、トランスクリプトミクス、プロテオミクス、メタボロミクスと呼ばれます。マルチオミクスではそれらの解析を組合わせて、複数の分子種を包括的に調べることを意味します。
※3 RNAシーケンス
オミクス解析のひとつであるトランスクリプトミクスはRNAの発現を対象とした解析です。トランスクリプトミクスの解析方法として、RNAシーケンスが最も主流な方法となっています。主にメッセンジャーRNA(mRNA)を対象として、全遺伝子の発現を網羅的に解析するものです。
※4 全ゲノム解析
全ゲノム解析(Whole genome sequencing; WGS)は、文字通り全ゲノムを対象とした、配列解読する解析手法です。全エクソーム解析で対象としない遺伝子間領域やイントロンまでも解析範囲となるため、全エクソーム解析では分からない遺伝子の異常を明らかにすることができます。
※5 全エクソーム解析
全エクソーム解析(Whole exome sequencing; WES)は、ゲノム中でもタンパク質をコードするエクソン領域を選択的に抽出して、配列解読する解析手法です。エクソンはタンパク質をコードするため極めて重要な領域であり、この領域に疾患原因が集積していると考えられます。しかし、エクソン領域は全ゲノムの約2%にすぎず、調べられていないゲノム領域が多く存在します。
※6 Alu因子
ゲノムの中には動きまわることが可能であるトランスポゾンが多く含まれることが知られています。その中でもAluは短鎖散在反復配列(SINE)に属しています。ヒトゲノムの10%程度がAlu因子からなると推定されています。これまでにもAlu因子の移動がヒトの病気やがんなどの発症に関わることが報告されていました。
※7 サンガーシーケンス
フレデリック・サンガーらが開発した遺伝子配列の解析方法です。上述の全エクソーム解析や全ゲノム解析に比べ、解析できる遺伝子断片は1つであり、解析の網羅性は低いが、対象となる領域が決まっている場合などにはより簡便は方法として用いられることが多いです。
【原著論文】
本研究はHuman Mutation誌のオンライン版で(2021年9月2日付)先行公開されました。
タイトル:
Genome sequencing and RNA-seq analyses of mitochondrial complex I deficiency revealed Alu insertion-mediated deletion in NDUFV2
タイトル(日本語訳):
ミトコンドリア呼吸鎖複合体I欠損症のゲノム解析とRNAシーケンスがNDUFV2遺伝子おけるAlu挿入が仲介する遺伝子欠失を明らかにした
著者:
Yoshihito Kishita1)2)、Masaru Shimura3)、Masakazu Kohda1)、Takuya Fushimi3)、Kazuhiro R Nitta1)、Yukiko Yatsuka1)、Shinichi Hirose4)、Hiroshi Ideguchi5)、Akira Ohtake6)7)、Kei Murayama1)3)8)、Yasushi Okazaki1)9)
著者(日本語表記):
木下 善仁1)2)、志村 優3)、神田 将和1)、伏見 拓矢3)、新田 和広1)、八塚 由紀子1)2)、廣瀬 伸一4)、井手口 博5)、大竹 明6)7)、村山 圭1)3)8)、岡﨑 康司1)9)
著者所属:
1)順天堂大学大学院難治性疾患診断・治療学講座/難病の診断と治療研究センター、2)近畿大学理工学部生命科学科、3)千葉県こども病院代謝科、4)福岡大学医学部総合医学研究センター、5)福岡山王病院小児科、6)埼玉医科大学小児科学・ゲノム医療学、7)埼玉医科大学難病センター、8)千葉県こども病院遺伝診療センター、9)国立研究開発法人理化学研究所生命医科学研究センター応用ゲノム解析技術研究チーム
DOI:10.1002/humu.24274
本研究は、JSPS科研費基盤研究B(JP19H03624)、JSPS新学術領域研究(JP20H05519)、AMED難治性疾患実用化研究事業(JP19ek0109273、JP18ek0109177、and JP21ek0109468)、AMED臨床ゲノム情報統合データベース整備事業((JP19kk0205014 and JP18kk0205002)、AMEDゲノム創薬基盤推進研究事業(JP21kk0305015)、文部科学省私立大学研究ブランディング事業、の支援を受け、多施設との共同研究の基に実施されました。
【関連リンク】
理工学部 生命科学科 講師 木下 善仁(キシタ ヨシヒト)
https://www.kindai.ac.jp/meikan/2456-kishita-yoshihito.html