筋萎縮性側索硬化症と前頭側頭型認知症の根本治療へ 異常なRNAを抑えるタンパク質群を発見

近畿大学医学部(大阪府大阪狭山市)内科学教室(脳神経内科部門)主任教授 永井 義隆、同助教 田港 朝也、近畿大学ライフサイエンス研究所特任講師 武内 敏秀らの研究グループは、大阪大学大学院医学系研究科(大阪府吹田市)神経内科学教授 望月秀樹、同精神医学教授 池田 学、同精神医学講師 森 康治らとの共同研究で、神経難病である筋萎縮性側索硬化症(ALS)と前頭側頭型認知症(FTD)の原因となる異常なRNA※1 のはたらきを抑えるタンパク質群を発見しました。さらに、これらのタンパク質が、ALSやFTDに対して治療効果をもたらすことを疾患モデル動物で証明しました。
本件に関する論文が、令和5年(2023年)1月16日(月)午前2:00(日本時間)に、分子遺伝学領域の国際的な学術誌"Human Molecular Genetics"にオンライン掲載されました。
【本件のポイント】
●筋萎縮性側索硬化症(ALS)と前頭側頭型認知症(FTD)の原因となる異常なRNAのはたらきを抑えるタンパク質群を発見
●これらのタンパク質がALSやFTDに対して治療効果を発揮することを、疾患モデル動物を用いて証明
●異常RNAを原因とするALSやFTDに対して、新たな治療法の開発につながる研究成果
【本件の内容】
筋萎縮性側索硬化症(ALS)は、全身の筋肉が急速に衰えてゆく神経疾患です。また、前頭側頭型認知症(FTD)は、アルツハイマー型認知症やレビー小体型認知症の次に多い変性性認知症※2 です。これらの神経難病は、まだ原因が十分には解明されておらず、根本的な治療法も開発されていませんが、近年、ALSとFTDの原因の一つが、異常なRNAのはたらきによるものであることが明らかとなりました。
本研究グループは、ALSとFTDの治療を目的として、疾患の根本的な原因となる異常なRNAの毒性を低下させる分子の探索を行いました。その結果、私たちがもともと持っている細胞内の一群のタンパク質が、異常なRNAに結合して、その量を減少させることを発見しました。また、これらのタンパク質が治療効果を発揮することを、疾患モデルのショウジョウバエを用いて証明しました。
本研究結果は、異常なRNAを原因とするALSやFTDに対し、新たな治療法の開発につながる成果です。
【論文概要】
掲載誌:
Human Moleculer Genetics(インパクトファクター:5.121@2021)
論文名:
Therapeutic reduction of GGGGCC repeat RNA levels by hnRNPA3 suppresses neurodegeneration in Drosophila models of C9orf72-linked ALS/FTD
(hnRNPA3は、異常なGGGGCCリピートRNAを減少させ、C9orf72関連ALS/FTDモデルショウジョウバエの神経変性を抑制する)
著者 :
田港 朝也1,3、武内 敏秀1,2,3※、上山 盛夫1,3、森 康治4、池田 学4、望月 秀樹5、永井 義隆1,2,3,5※ ※ 責任著者
所属 :
1 近畿大学医学部内科学教室(脳神経内科部門)、2 近畿大学ライフサイエンス研究所、3 大阪大学大学院医学系研究科神経難病認知症探索治療学寄附講座、4 大阪大学大学院医学系研究科精神医学、5 大阪大学大学院医学系研究科神経内科学
【研究詳細】
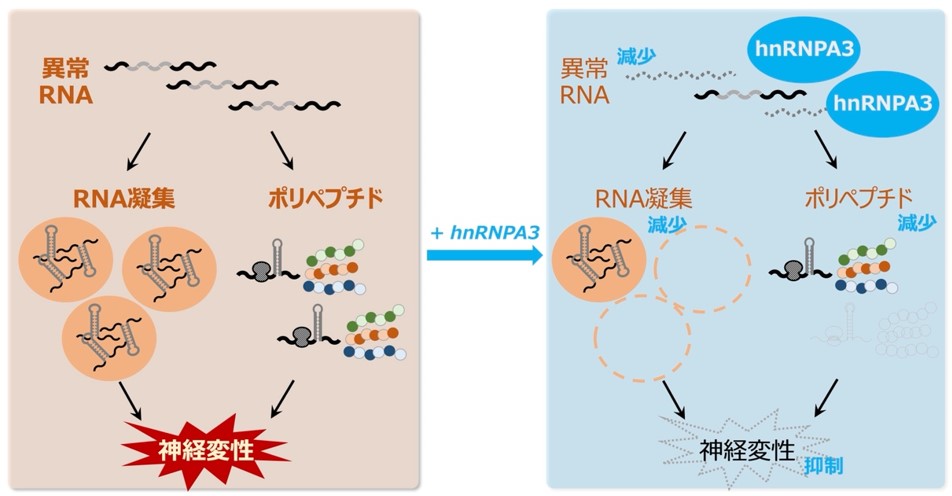
近年、一部の筋萎縮性側索硬化症(ALS)および前頭側頭型認知症(FTD)において、C9orf72と呼ばれる遺伝子の異常が、最も多い原因遺伝子異常であるという報告がなされました。C9orf72遺伝子領域内には、「GGGGCC」というDNA6塩基(G:グアニン、C:シトシン)が複数回繰り返された配列が存在しますが、ALSやFTDの患者では繰り返し配列が異常に長く連なっています(健常者:2~23回、患者:700~1600回)。この異常に長い繰り返し配列を持つ遺伝子から転写※3 された異常なRNAは、細胞内のタンパク質を巻き込んで凝集したり、異常なポリペプチドへと翻訳※4 されたりすることで、本来の細胞活動に悪影響を与え、神経細胞の機能障害や細胞死を招くと考えられています。
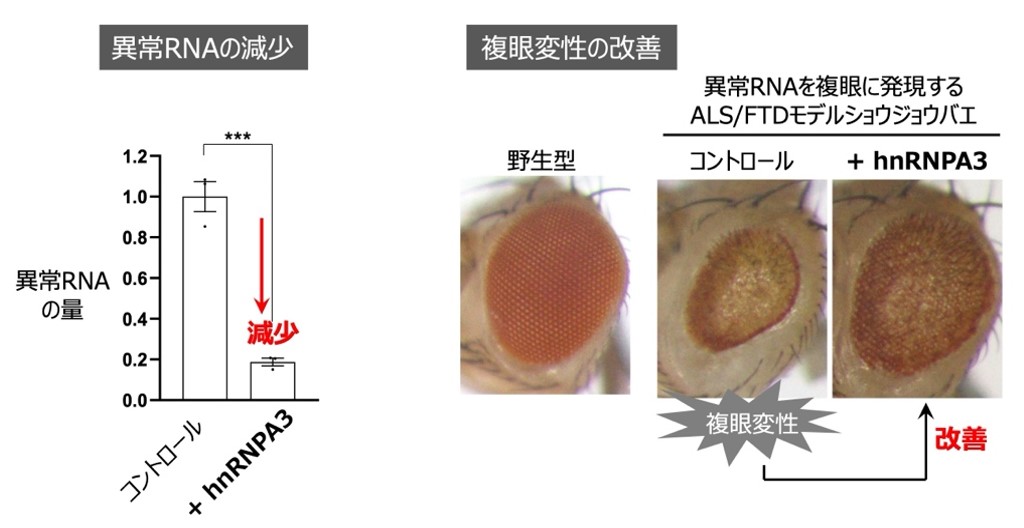
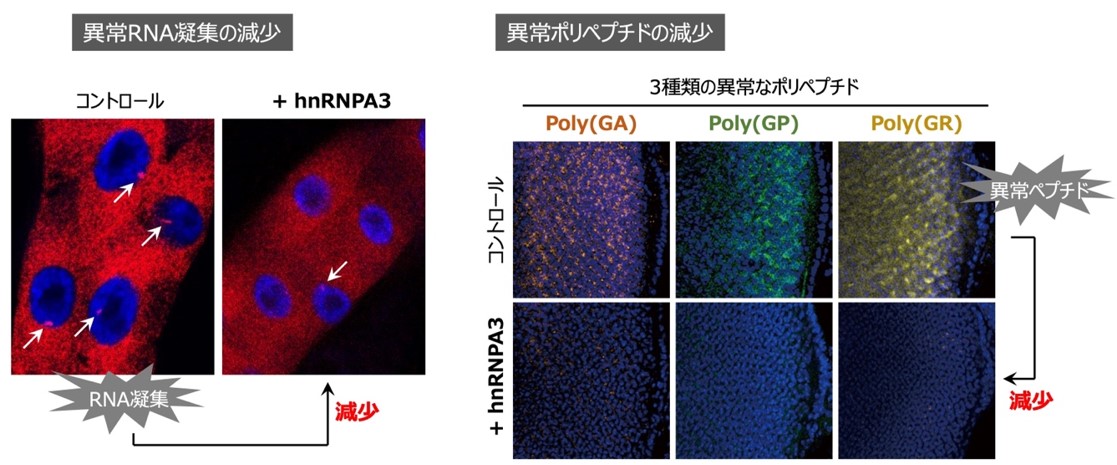
本研究グループは、疾患の根本原因となる異常RNAのはたらきを抑えることが、ALSおよびFTDの治療につながるのではないかと考え、実験を行いました。その結果、hnRNPA3をはじめとする細胞内に存在する複数のタンパク質が、異常RNAの量を大きく減少させるはたらきを持つことを発見しました。さらに、これらのタンパク質は、異常なRNA凝集や異常なポリペプチド合成を抑え、神経変性を抑えることを、ALSおよびFTDモデルショウジョウバエを用いて証明しました。
本研究結果は、異常なRNAを原因とするALSやFTDに対し、新たな治療法の開発につながる成果です。


【研究者のコメント】
氏名 :永井 義隆
所属 :近畿大学医学部 医学科 内科学教室(脳神経内科部門)
職位 :主任教授
学位 :博士(医学)
コメント:C9orf72遺伝子内のGGGGCC繰り返し配列の異常は欧米人では最も多い筋萎縮性側索硬化症および前頭側頭型認知症の原因遺伝子異常です。他にも、CTGやCGG、TGGAAなどの繰り返し配列の異常が、脊髄小脳失調症や神経核内封入体病などの神経変性疾患の原因として見つかっており、これらはリピート(繰り返し)病と呼ばれています。今回の研究は、このような繰り返し配列から転写される異常RNAの量を減少させるタンパク質を初めて発見したものであり、同じような方法で脊髄小脳失調症などの他の疾患の治療法の開発につながる可能性にも期待しています。
【研究支援】
本研究は、JSPS科学研究費助成事業学術変革領域研究(A)(20H05927)、同基盤研究(B)(21H02840)、およびAMED難治性疾患実用化研究事業(JP20ek0109316)の一環として行われました。
【用語解説】
※1 RNA:DNAとよく似た化学構造を持つ物質(リボ核酸)で、DNAを鋳型として合成される。RNAは、タンパク質が合成されるもとになったり、遺伝子の働きを変化させたりするなど、細胞活動に重要な役割を持つ一方で、異常なRNAは生存に悪影響をもたらす。
※2 変性性認知症:神経細胞の機能障害や細胞死により引き起こされる認知症。
※3 転写:DNAからRNAが合成されること。DNA上の遺伝情報をもとにタンパク質を合成する際、いったんDNAからRNAに情報をコピーすることをいう。
※4 翻訳:RNAに転写された遺伝情報をもとに、タンパク質を合成すること。
【関連リンク】
医学部 医学科 教授 永井 義隆(ナガイ ヨシタカ)
https://www.kindai.ac.jp/meikan/2687-nagai-yoshitaka.html
医学部
https://www.kindai.ac.jp/medicine/
近畿大学ライフサイエンス研究所
https://www.med.kindai.ac.jp/life/