デュアル光コムを用いたバイオセンシングに成功(世界初) ~生体分子の高感度・迅速検出に期待~
徳島大学ポストLEDフォトニクス研究所、徳島大学大学院先端技術科学教育部、高知工科大学システム工学群の共同研究グループは、デュアル光コムを用いたバイオセンシングに成功しました。
ポイント
・バイオセンシングは、新型コロナ感染症ウイルスを始めとした生体分子の検出に有用であるが、高感度性と迅速性を両立するのが困難であった。
・光コムの光/電気周波数変換と、デュアル光コムのアクティブ・ダミー温度補償を用いて、新型コロナウイルスの迅速・高感度検出を実現した。
・今後、感染症病原体、健康バイオマーカー、食品汚染物質、環境ホルモン等の超早期検出が可能になり、各種の予防対策に貢献すると期待される。
報道概要
バイオセンサー(注1)は、生体の巧みな分子識別機能を利用あるいは模倣した生体分子センサーで、医療・食品・環境分野など幅広い分野に応用されています。特に、測定対象分子と分子識別部の相互作用を光学的に読み出す光バイオセンサーは、高い定量性や簡易・迅速計測が特徴ですが、新型コロナウイルスやがん細胞の超早期検出を実現するためには感度が不十分でした。
徳島大学ポストLEDフォトニクス研究所の安井武史教授・加治佐平客員准教授(令和5年3月退職)らと、徳島大学大学院先端技術科学教育部の宮村祥吾大学院生(博士後期課程)、高知工科大学システム工学群の田上周路准教授の研究グループは、上記の課題を解決するため、次世代レーザーとして注目されている光周波数コム(光コム)(注2)を光源としてではなくセンサーとして用いることにより、世界で初めてバイオセンシング(注3)に応用しました。本研究では、光周波数で高感度センシングして電気周波数で高精度読み出しを行うと共に、双子の光コム(デュアル光コム)を用いてセンサー信号の温度ドリフト(注4)をアクティブ・ダミー温度補償(注5)して測定環境温度の影響を抑えることにより、新型コロナウイルスの迅速・高感度検出を実現しました。
本手法により、新型コロナウイルスのような新興・再興感染症ウイルスのみならず、がんを始めとした健康バイオマーカー、健康被害に繋がる食品や環境の汚染物質などの超早期検出が期待されます。
詳細はこちらをご覧ください。
徳島大学ポストLEDフォトニクス研究所
安井研究室YouTubeチャンネルによる説明動画
https://youtu.be/sPMhvJLi3S8?si=EERnRiEEUX-jwu1A
研究の背景と経緯
生物由来のさまざまな化学物質(糖/核酸/タンパク質など)を検出可能なバイオセンサーは、生体の巧みな分子識別機能を利用あるいは模倣した生体分子センサーで、糖尿病の血糖センサーをはじめ、医療・食品・環境分野など幅広い分野に応用されています。特に、光を用いたバイオセンサー(光バイオセンサー)は高精度や迅速計測が特徴ですが、更なる高感度化が求められています。もし、光バイオセンサーの感度を大幅に向上できれば、新型コロナウイルスやがんの超早期検出が実現可能になると考えられます。感度の大幅向上のためには、これまでとは本質的に異なる技術的アプローチの導入が必要不可欠です。
従来の光バイオセンシングでは、光で高感度センシングを行い、光周波数(光スペクトル)信号で計測を行っていましたが、光周波数計測装置の性能限界が高感度化を制約していました。もし、光で高感度センシングを行いながら電気周波数(電気スペクトル)信号で読み出しを行うことができれば、高性能な電気周波数計測機器を利用することができます。そこで、光周波数信号を電気周波数信号に正確に変換する手段として、『光周波数コム(光コム)』に着目しました。
研究の内容と成果
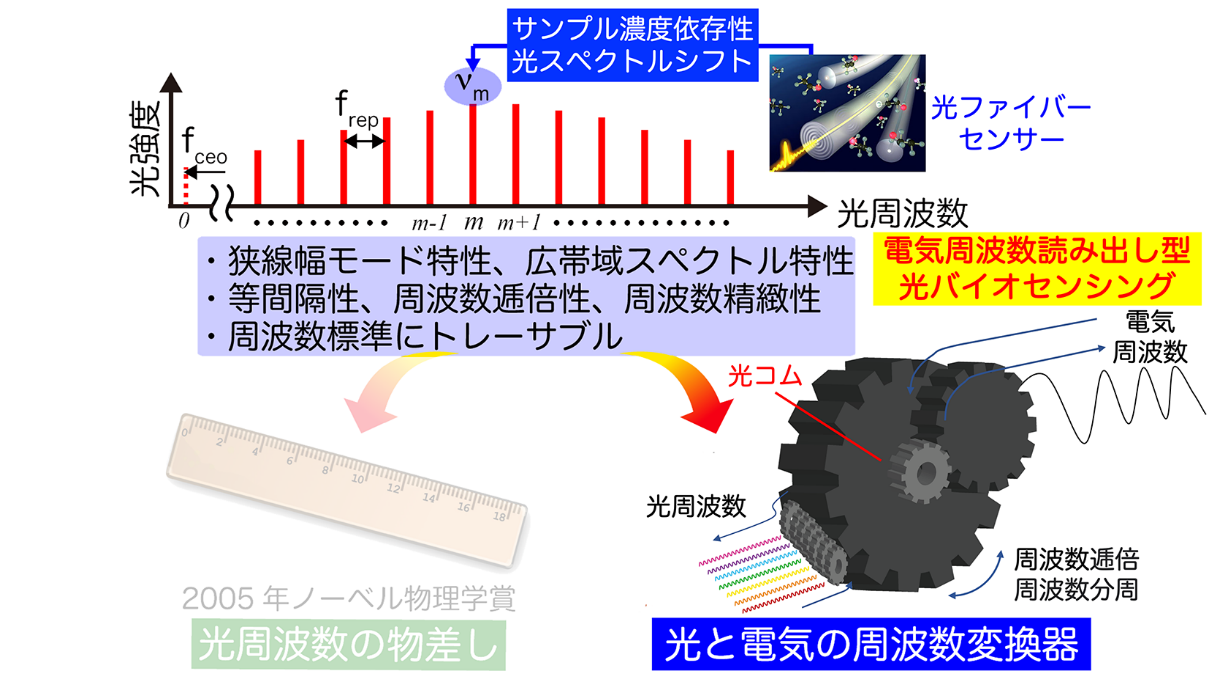
光コムは、多数の光周波数モード列(光コム・モード)が等間隔で櫛(Comb:コム)の歯状に並んだ超離散マルチスペクトルを有しています(図1上段)。この光コムを用いると、高精度な電気周波数信号を光周波数信号に変換することが可能になり、「光周波数(波長)の物差し」としてガス分析等に利用されてきました(図1左下)。一方、光コムは、光周波数信号を電気周波数信号に変換する手段としても利用できます。本研究では、光コムにファイバーバイオセンサーを組み込むことにより、サンプル濃度依存性の光周波数シフトを電気周波数シフトに変換しました(図1右下)。電気周波数信号は、最高精度の国家基準が整備され、高性能・低価格な計測機器も充実しているので、高精度・高速・簡便な計測が可能です。『光コムの光/電気周波数変換』と『高精度な電気周波数計測』を上手く組み合わせることにより、光の高感度センシング性を有しながら、取り扱いが容易で高精度な電気周波数読み出し型の光バイオセンシング(バイオセンシング光コム)が可能になります。

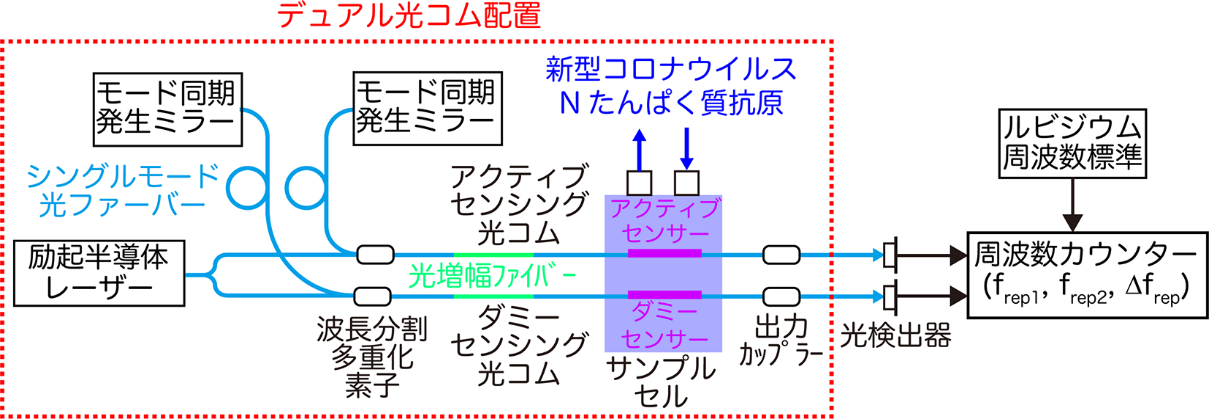
バイオセンシング光コムの残された課題は、センサー信号の温度ドリフトです。センサー信号は、サンプルの濃度変化以外に、環境温度変化の影響(温度ドリフト)を受けます。この温度ドリフトを抑制するため、アクティブ・ダミー温度補償を用いました(図2)。この手法では、性能が同じファイバー光コム共振器をペアで準備し(デュアル光コム配置)、一方にサンプル濃度変化と温度変化の両方に反応するアクティブ・センサーを組み込み(アクティブ・センシング・光コム、センサー信号frep1)、他方に温度変化のみに反応するダミー・センサーを組み込んで(ダミー・センシング・光コム、モード間隔frep2)、両センサーを同一のサンプルセルに配置します。この場合、アクティブ・センサーのみがサンプル濃度変化に対して感度を持つのに対し、温度ドリフトの影響は両センサーに同様な振る舞いとして現れます。従って、アクティブ・センシング・光コムとダミー・センシング・光コムの差分信号(△frep=frep1-frep2)を計測することにより、温度ドリフトの影響を相殺し、サンプル濃度依存性信号のみを抽出することが可能になります。

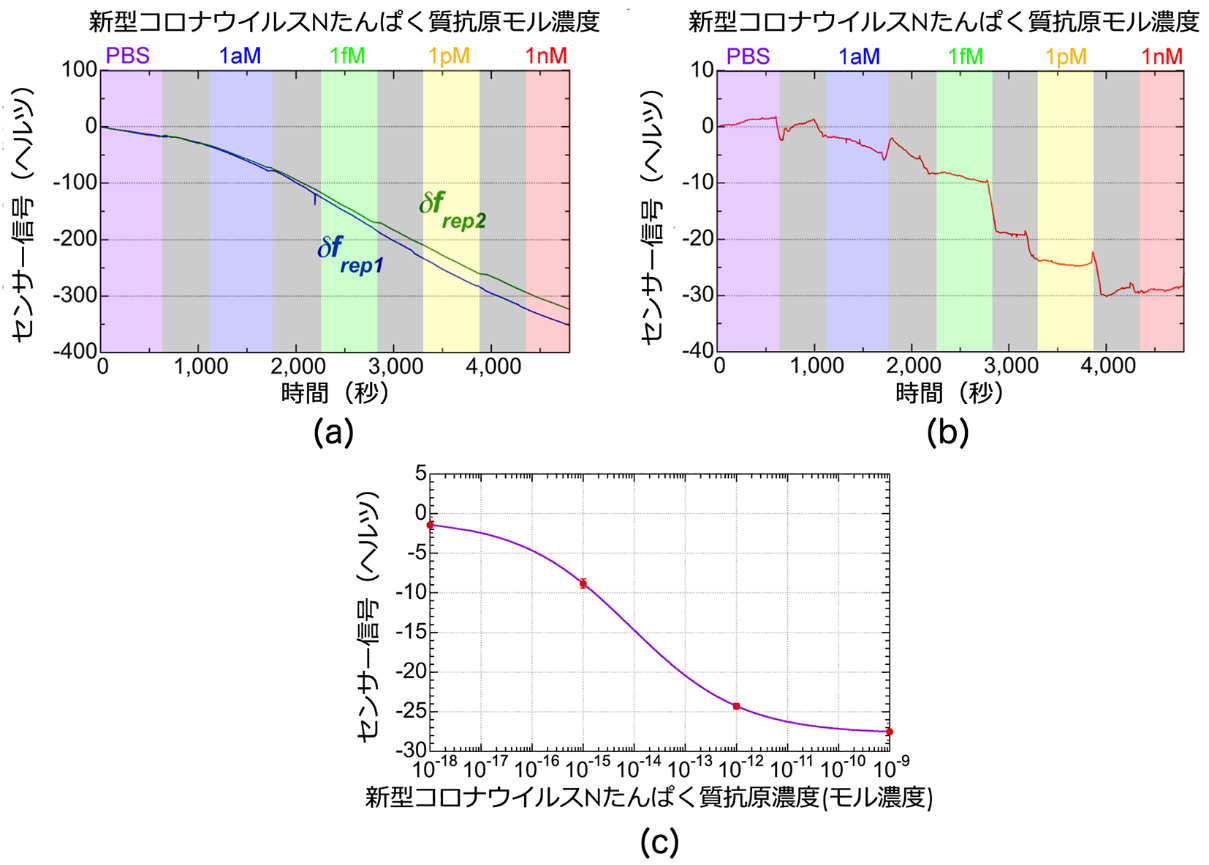
今回は、リン酸緩衝生理食塩水(PBS)中の新型コロナウイルスN(ヌクレオカプシド)たんぱく質抗原濃度を10分刻みでステップ状に変化させながら、計測を行いました。図3(a)は、アクティブ・センシング・光コムとダミー・センシング・光コムのセンサー信号(frep1、frep2)の変化を示しています。両センサー信号において、温度ドリフトによる緩やかな変化が確認される一方で、アクティブ・センシング・光コムではサンプル濃度依存性のステップ状変化が確認されていません。これは、サンプル濃度変化によるfrepシフトよりも温度ドリフトによるfrep変動が大きいことに起因しています。そこで、両者の差分信号(△frep)を抽出したのが、図3(b)になります。温度ドリフトが抑制され、サンプル濃度依存性のステップ状変化が確認できました。この測定結果から、モル濃度とセンサー信号の関係性をグラフしたのが、図3(c)の赤丸プロットになります。実験結果の妥当性を評価するため、理論モデル関数を用いてカーブフィッティング解析を行ったところ(紫ライン)、10分の測定時間で、検出限界のモル濃度が37aMであることを確認しました。

役割分担
・徳島大学 :システム基本設計・構築、実証実験
・高知工科大学:ファイバーセンサー設計
今後の展開
今回は、PBS中に新型コロナウイルスNたんぱく質抗原のみが存在する理想的条件での計測でしたが、実際のサンプル(唾液、鼻咽頭ぬぐい液、鼻腔ぬぐい液など)では不要なたんぱく質(夾雑物)が多く含まれ、これらの非特異的なセンサー表面吸着により感度や精度が制限されます。今後は、実際のサンプルを想定して、非特異吸着を避けるセンサー表面修飾法の導入等を検討し、より現実に近い条件での性能評価を行う予定です。
用語解説
(注1)バイオセンサー
バイオセンサーは、生物学的または生化学的プロセスを検出し、それを電気信号、光学信号、または他の形式の信号に変換する装置またはセンサーです。一般的には、生体由来の分子(酵素や抗体)をセンサー表面に固定し、ターゲット分子が結合するとその変化を検出します。高感度な検出能力と迅速な測定を利用して、健康や疾病に関連した血糖やたんぱく質、環境や食品の安全を脅かす有害物質や細菌、最近では新型コロナウイルスを検出することに利用されています。
(注2)光周波数コム(光コム)
光コムは、数万本から数十万本にも及ぶ狭線幅なレーザー光(光周波数モード)が等間隔で櫛(comb:コム)の歯状に整然と並んだ離散・マルチスペクトル構造を持っています(図1上段)。周波数安定化制御により、光コムを構成する全ての光周波数モードの絶対周波数を厳密に決定できることから、光スペクトルにおける「光周波数の物差し」としてガス分光分析等で利用されてきました。今回は、光コムを「光/電気周波数変換器」として利用することにより、光コムの新しい応用展開がバイオセンシング分野で期待されます。
(注3)バイオセンシング
バイオセンシングは、バイオセンサーを使用して生物学的または生化学的プロセスを検出、監視、または測定する一連の技術、方法、またはアプローチを指します。バイオセンシングは、バイオセンサーを活用してデータを収集し、解釈するプロセス全体を含みます。
(注4)温度ドリフト
バイオセンシングにおける温度ドリフトは、バイオセンサー自体または生体試料の温度変化が、バイオセンサーの測定結果に影響を与える現象を指します。温度ドリフトは、バイオセンサーが正確な測定を行う際に考慮しなければならない重要な要因です。
(注5)アクティブ・ダミー温度補償
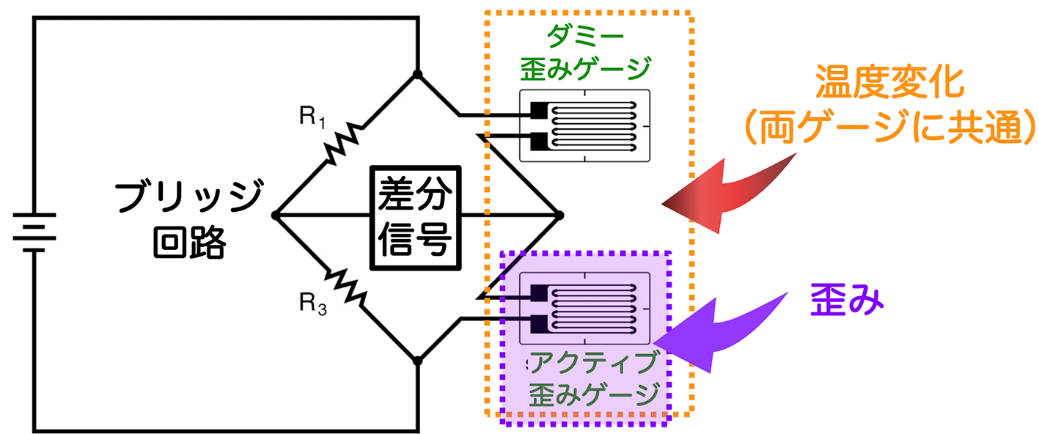
アクティブ・ダミー温度補償は、歪みゲージ(歪みセンサー)の温度補償に一般に使われる技術です。歪みゲージは、歪みと温度の両方に感度があるため、温度変化のある測定環境での歪みを正確に計測することは困難でした。そこで、性能が等価な一対の歪みゲージを準備し、一方を歪み計測部位に取り付け(アクティブ歪みゲージ)、他方をその近傍で歪みが発生しないが温度変化は同等な部位に貼りつけます(ダミー歪みゲージ)。アクティブ歪みゲージは歪みと温度変化の両方を計測するのに対し、ダミー歪みゲージは温度変化のみを計測するので、両者の差分信号をブリッジ回路で算出することにより、温度変化の影響が相殺され、歪みのみ計測が可能になります(図A)。

謝辞
本研究は、科学研究費助成事業(22H00303)、日本医療研究開発機構(20he0822006j00)、科学技術振興機構(JPMJMS2025)、内閣府・地方大学・地域産業創生交付金事業[徳島県「次世代“光”創出・応用による産業振興・若者雇用創出計画(次世代ひかりトクシマ)」]、および徳島大学研究クラスター事業(2201001)の支援を受けて実施されました。
論文情報
掲載誌:Scientific Reports
論文名:Rapid, high-sensitivity detection of biomolecules using dual-comb biosensing
著者名:Shogo Miyamura, Ryo Oe, Takuya Nakahara, Hidenori Koresawa, Shota Okada, Shuji Taue, Yu Tokizane, Takeo Minamikawa, Taka-Aki Yano, Kunihiro Otsuka, Ayuko Sakane, Takuya Sasaki, Koji Yasutomo, Taira Kajisa, and Takeshi Yasui
DOI番号:10.1038/s41598-023-41436-3
関連特許
関連特許3件出願済