解熱鎮痛薬アスピリンと低酸素環境が「PIK3CA変異型大腸がん」の細胞内グルタミン蓄積を促進 ~細胞内に蓄積したグルタミンを標的とした新たな治療戦略へ~

【発表のポイント】
●低酸素環境下において、アスピリンがPIK3CA変異型大腸がん細胞内のグルタミン蓄積を特異的に促進することを発見
●アスピリンとグルタミン輸送阻害剤の併用により、がん細胞の増殖を抑え込む強力な抗腫瘍効果を実証
●既存薬(アスピリン)の抗腫瘍効果を最大化させる、大腸がんに対する新たな併用治療戦略の開発に期待
学校法人関西医科大学(大阪府枚方市 理事長・山下敏夫、学長・木梨達雄)附属病院臨床腫瘍科 診療講師 朴将源、近畿大学(学長・松村到)薬学部医療薬学科准教授 山本哲志、京都府公立大学法人京都府立医科大学(理事長・金田章裕、学長・夜久均)大学院医学研究科分子標的予防医学講師 渡邉元樹らの研究チームは、実際のがん組織に近い「低酸素環境」において、解熱鎮痛薬のアスピリンが、特定の遺伝子変異(PIK3CA変異)を持つ大腸がん細胞内へのグルタミン(アミノ酸)の蓄積を特異的に促進することを明らかにしました。グルタミンの蓄積は、がん代謝阻害剤による重要な治療標的となります。この結果により、既存薬であるアスピリンの抗腫瘍効果を最大化させる新たな併用治療戦略の糸口となることが期待されます。
なお、本研究をまとめた論文が『Scientific Reports』(インパクトファクター:3.9)に3月24日(火)19時付で掲載されました。
【書誌情報】
掲載誌 :『Scientific Reports』DOI: 10.1038/s41598-026-42753-z
論文タイトル:Hypoxia and aspirin additively increase intracellular glutamine accumulation
in PIK3CA-mutated colorectal cancer cells.
(PIK3CA大腸がん細胞においてアスピリンは低酸素刺激と相加的に
細胞内グルタミン蓄積を増強する)
筆者 :関西医科大学 医学部 乳腺外科学講座 梅嵜乃斗香
関西医科大学附属病院 臨床腫瘍科 朴将源
関西医科大学 附属生命医学研究所綜合研究施設 松尾禎之
近畿大学 薬学部 医療薬学科 山本哲志
高知大学 医学部 腫瘍内科学講座 佐竹悠良
京都府立医科大学大学院医学研究科 分子標的予防医学 渡邉元樹
南魚沼市民病院附属城内診療所 広田喜一
関西医科大学香里病院 化学療法センター 杉江知治
箕面市立病院 関本貢嗣
【本研究の背景】
日常的に使用される解熱鎮痛薬である「アスピリン」は、近年、がん(特に大腸がん)の予防や治療薬として転用する「ドラッグ・リポジショニング※1」の候補として大きな注目を集めています。これまでの臨床データから、特定の遺伝子「PIK3CA※2」に変異を持つ大腸がん患者において、アスピリンが特に有効であることが分かっています。研究グループは以前の研究で、アスピリンの抗腫瘍効果が、がん細胞の生存に欠かせないアミノ酸である「グルタミン※3」の代謝と密接に関わっていることを明らかにしていました。しかし、実際の体内におけるがん組織の内部は酸素が極めて少ない「低酸素」という特殊な環境にあり、そのような腫瘍の微小環境下で、アスピリンががん細胞にどのようなメカニズムで影響を与えているのかは十分に解明されていませんでした。
【本研究の概要】
本研究では、低酸素環境という実際のがん組織に近い条件下で、アスピリンがPIK3CA変異型大腸がん細胞のグルタミン代謝にどのような影響を及ぼすのかを詳細に調査しました。遺伝子の働きを網羅的に調べるRNAシーケンス※4 や、細胞内の代謝物を直接測定する標的メタボロミクス※5 などの最新手法を用い、アスピリン処理および低酸素刺激を与えたPIK3CA変異型大腸がん細胞の反応を、変異を持たない正常な(野生型)細胞と比較しました。さらに、がん細胞が外部からグルタミンを取り込むための「トランスポーター※6」の働きをブロックする阻害剤(V-9302)を用い、アスピリンとの併用による抗腫瘍効果も検証しました。
【本研究の成果】
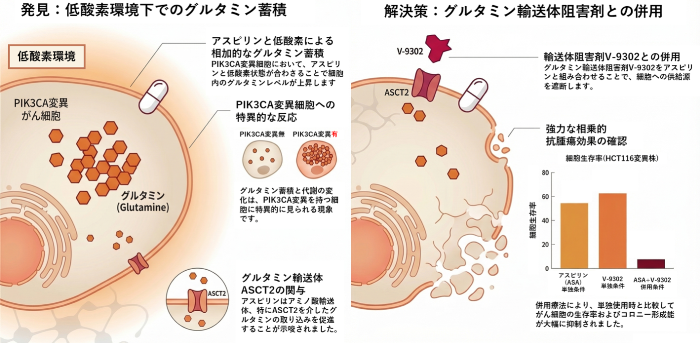
遺伝子発現の解析結果から、低酸素環境下でアスピリンを投与すると、PIK3CA変異を持つ大腸がん細胞に特異的に、アミノ酸(グルタミンなど)の取り込みに関わる経路の働きが活発になることが判明しました。実際に細胞内の代謝物を測定したところ、アスピリン投与と低酸素刺激が相加的に働き、がん細胞内に顕著にグルタミンが蓄積することが実証されました。さらに、グルタミンを細胞内に取り込むトランスポーター(ASCT2)を阻害する薬剤である「V-9302」をアスピリンと併用した結果、細胞内へのグルタミンの過剰な蓄積が抑えられるとともに、アスピリン単独での投与と比較して、がん細胞の増殖をより強力に抑え込む(相乗的な抗腫瘍効果)ことができると確認されました。本研究の成果は、低酸素環境下においてアスピリンががん細胞のグルタミン蓄積を促すことを明らかにしたものであり、グルタミン輸送を標的とする薬剤を組み合わせることで、アスピリンの大腸がんに対する治療効果をさらに飛躍的に高められる可能性(新たな併用療法の開発)を示す重要な発見です。
【用語解説】
※1 ドラッグ・リポジショニング(既存薬再開発)
すでに別の病気の治療薬として承認・使用されている薬(本研究における解熱鎮痛薬の「アスピリン」など)が持つ新たな薬効を見出し、がんの予防や治療など、異なる疾患の薬として転用・再開発する手法です。非ステロイド性抗炎症薬(NSAIDs)であるアスピリンは、大腸がんに対する再開発薬として大きな可能性を秘めています。
※2 PIK3CA
大腸がん患者の約10~20%に認められる遺伝子変異です。これまでの多くの臨床データから、この変異を持つ大腸がん患者に対してはアスピリンによる再発予防効果などが高いことが示されており、薬の効き目を予測する有望な指標となっています。また、PIK3CA変異を持つ大腸がん細胞は、自身の生存のためにグルタミン代謝の経路を変化させることが分かっています。
※3 グルタミン
腫瘍の成長や生存において極めて重要な役割を果たすアミノ酸の一種です。通常時だけでなく、がん組織内部のような酸素が乏しい「低酸素環境」においても、がん細胞が増殖するためのエネルギー源や、細胞内の恒常性を保つための重要な栄養素として利用されます。
※4 RNAシーケンス
細胞から抽出したRNAの配列を読み取り、どの遺伝子がどれくらい働いているか(発現しているか)を網羅的に調べる解析技術です。
※5 メタボロミクス
細胞内に存在するアミノ酸などの代謝物質の種類や量を、網羅的かつ直接的に測定する分析手法です。本研究では質量分析器(LC-MS/MS)を用いた「標的メタボロミクス」手法によって、アスピリン投与や低酸素刺激が細胞内のグルタミン量に与える影響を正確に定量しています。
※6 トランスポーター
細胞の表面(膜)に存在し、細胞の外からグルタミンなどのアミノ酸を細胞内に取り込む「通り道」となるタンパク質です。
【関連リンク】
薬学部 医療薬学科 准教授 山本哲志(ヤマモトテツシ)
https://www.kindai.ac.jp/meikan/429-yamamoto-tetsushi.html