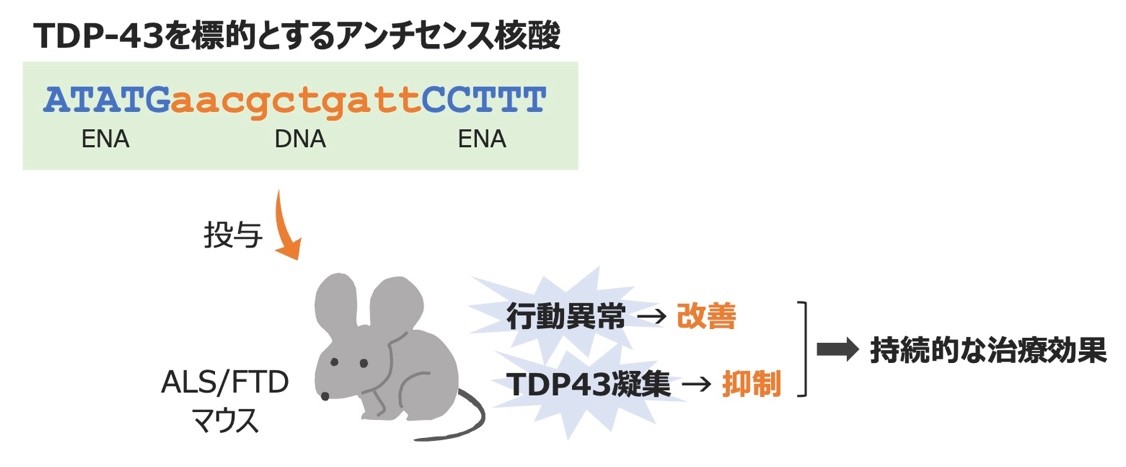
筋萎縮性側索硬化症と前頭側頭型認知症の核酸医薬を開発 発症に関与するタンパク質の異常凝集を抑制し、治療効果を発揮

近畿大学医学部(大阪府大阪狭山市)内科学教室(脳神経内科部門)主任教授 永井 義隆、近畿大学ライフサイエンス研究所特任講師 武内 敏秀らの研究グループは、大阪大学大学院医学系研究科(大阪府吹田市)神経内科学教授 望月 秀樹、神戸天然物化学株式会社(兵庫県神戸市)執行役員 医薬フロンティア部部長 閨 正博、名古屋大学大学院医学系研究科(愛知県名古屋市)特任教授(現:愛知医科大学学長)祖父江 元らとの共同研究で、神経難病である筋萎縮性側索硬化症(ALS)と前頭側頭型認知症(FTD)の発症に関与するタンパク質TDP-43※1 の遺伝子を標的とした核酸医薬※2 を開発しました。さらに、この核酸医薬が、ALSやFTDに対して治療効果をもたらすことを、疾患モデルマウスを用いて証明しました。
本件に関する論文が、令和5年(2023年)2月1日(水)に、分子治療学領域の国際的な学術誌"Molecular Therapy-Nucleic Acids"にオンライン掲載されました。
【本件のポイント】
●筋萎縮性側索硬化症(ALS)と前頭側頭型認知症(FTD)の発症に関与するタンパク質TDP-43の遺伝子を標的とした核酸医薬を開発
●開発した薬が、タンパク質TDP-43の異常凝集を抑制し、ALSやFTDに対して治療効果を発揮することを、疾患モデルマウスを用いて証明
●ALSやFTDに対し、新たな治療法の開発につながる研究成果
【本件の内容】
筋萎縮性側索硬化症(ALS)は、全身の筋肉が急速に衰えていく神経疾患です。また、前頭側頭型認知症(FTD)は、アルツハイマー型認知症やレビー小体型認知症の次に多い変性性認知症※3 です。これらの神経難病は、まだ原因が十分には解明されておらず、根本的な治療法も開発されていません。
近年、ほぼすべてのALS患者と半数程度のFTD患者において、TDP-43というタンパク質が神経細胞内で異常に凝集・蓄積したり、細胞内で通常とは異なる場所に存在したりすることが明らかとなりました。
研究グループは、多くのALSとFTDに共通の根本原因と考えられるタンパク質TDP-43の異常な凝集・蓄積を抑制するために、TDP-43の遺伝子を標的とした核酸医薬の開発を行いました。開発した核酸医薬は、疾患モデルマウスにおいてTDP-43の凝集を抑制し、1回の投与で持続的な治療効果を発揮することが確認されました。
本研究成果は、TDP-43を標的とした核酸医薬の有効性を初めて示すものであり、今後、安全性を十分に検証した上でヒトでの臨床研究を実施することによって、ALSやFTDに対する新たな治療法の開発につながると期待されます。
【論文概要】
掲載誌:
Molecular Therapy-Nucleic Acids
(インパクトファクター:10.18@2021-2022)
論文名:
Sustained therapeutic benefits by transient reduction of TDP-43 using ENA-modified antisense oligonucleotides in ALS/FTD mice
(TDP-43を標的としたENA修飾アンチセンス核酸は、ALS/FTDモデルマウスに対して単回投与で持続的な治療効果をもたらす)
著者:
武内 敏秀1,2,3※、前田 和宏3、Ding Xin1,3、大江 由佳子3、武田 明子1,3、井上 真奈1、長野 清一3,4、藤原 健志5、松田 誠司5、石垣 診祐6、佐橋 健太郎6、皆川 栄子7、望月 秀樹4、閨 正博5、祖父江 元6、永井 義隆1,2,3,4※ ※ 責任著者
所属:
1 近畿大学医学部内科学教室(脳神経内科部門)、2 近畿大学ライフサイエンス研究所、3 大阪大学大学院医学系研究科神経難病認知症探索治療学寄附講座、4 大阪大学大学院医学系研究科神経内科学、5 神戸天然物化学株式会社、6 名古屋大学大学院医学系研究科脳神経内科学、7 国立精神・神経医療研究センター神経研究所
【研究詳細】
本研究では、筋萎縮性側索硬化症(ALS)および前頭側頭型認知症(FTD)の治療法開発を目的として、発症に深く関与すると考えられるタンパク質TDP-43の遺伝子を標的としたGapmer型※4 アンチセンス核酸※5 の開発を行いました。Gapmer型アンチセンス核酸は20塩基長程度で、両端に修飾核酸※6 を数塩基、中央にはDNAを配置した構造の核酸です。これが標的タンパク質のmRNAに結合すると、細胞内の特殊な酵素によりmRNAが切断され、標的タンパク質の合成が抑制されると考えられています。
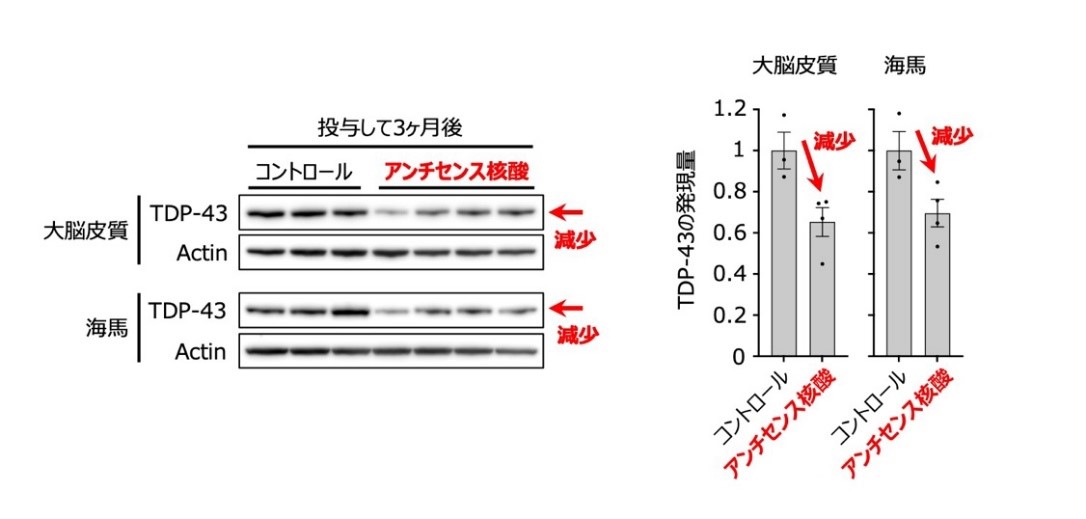
まず、Gapmer型アンチセンス核酸のRNAへの結合性および生体内安定性を高めるため、ENAs(2’-O,4’-C-ethylene nucleic acids)と呼ばれる修飾核酸を用いました。また、TDP-43の細胞内発現量を効率よく減少させる標的配列を見つけるため、TDP-43のmRNA全長に対し、標的配列の異なるGapmer型アンチセンス核酸を多数設計し、培養細胞を用いてひとつずつ検証を行いました。その結果、得られたGapmer型アンチセンス核酸は、培養細胞にてTDP-43の発現量を大きく減少させるとともに、ALS/FTDモデルマウスに対しても、脳室内への単回投与で3カ月間にわたりTDP-43発現を抑制することが確認されました。さらに、この核酸を投与されたモデルマウスは、神経細胞内のTDP-43の異常凝集や局在異常が抑制されるとともに、運動機能障害や不安行動などの疾患と関連する行動異常が抑制されるなど、長期にわたり治療効果を示すことが確認されました。
本研究により、TDP-43を標的とした核酸医薬がALS/FTD治療に有効である可能性が示されました。一方、TDP-43は細胞内で重要な働きを持つ分子であるため、今回の核酸医薬が毒性・安全性に影響しないかどうかを十分に検証する必要があります。今後、臨床応用する上での課題を解決し、ヒトでの臨床研究を実施することで、ALSやFTDに対する新たな治療法の開発につながると期待されます。


【研究者のコメント】
永井 義隆(ながい よしたか)
所属 :近畿大学医学部医学科内科学教室(脳神経内科部門)
職位 :主任教授
学位 :博士(医学)
コメント:
ALSやFTDだけでなく、アルツハイマー病やパーキンソン病などの神経変性疾患において、様々な原因タンパク質が明らかになっています。最近、これらの原因タンパク質の遺伝子を標的とした核酸医薬の開発研究が進み、脊髄性筋萎縮症に対する核酸医薬は既に実用化されています。今回の研究は、ほとんどのALS患者と半数程度のFTD患者の原因となるTDP-43の凝集を抑制する世界初の核酸医薬を開発したものであり、ヒトに対する有効性および安全性を確認したうえで、実用化につながることを期待しています。
【研究支援】
本研究は、AMED脳科学研究戦略推進プログラム(融合脳)(JP20dm0107061)の一環として行われました。
【用語解説】
※1 TDP-43:RNAやDNAに結合するタンパク質。通常は主に細胞の核内に存在する。ほぼすべてのALS患者と半数程度のFTD患者において、細胞質内で異常な凝集・蓄積が認められる。
※2 核酸医薬:DNAやRNAなどの核酸を基本の構造とする薬物。
※3 変性性認知症:神経細胞の機能障害や細胞死により引き起こされる認知症。
※4 Gapmer型:両端部に修飾核酸を3~5塩基程度配置し、中央部にはDNAを配置した構造。
※5 アンチセンス核酸:標的とする核酸に対して相補的な配列を有する核酸。標的核酸に特異的に結合し、分解やスプライシング(mRNAの前駆体に含まれるタンパク質合成に不要な部分が除かれ、必要部分が再連結する反応)阻害などを引き起こす。
※6 修飾核酸:人工的な化学修飾を有する核酸。
【関連リンク】
医学部 医学科 教授 永井 義隆(ナガイ ヨシタカ)
https://www.kindai.ac.jp/meikan/2687-nagai-yoshitaka.html
医学部
https://www.kindai.ac.jp/medicine/
近畿大学ライフサイエンス研究所
https://www.med.kindai.ac.jp/life/