クローン胚が早期発生停止となる原因遺伝子を発見 クローン胚の早期発生停止を防止し、ゲノム保全技術発展などに寄与

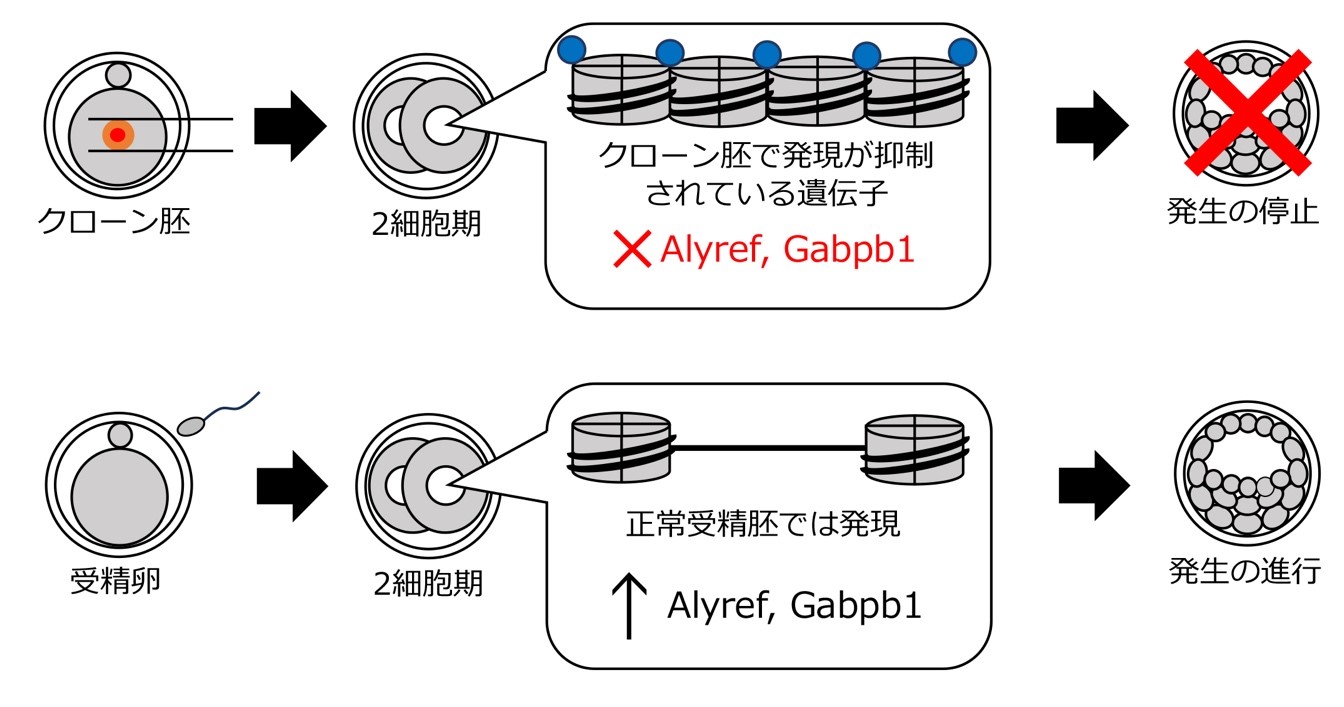
近畿大学生物理工学部(和歌山県紀の川市)遺伝子工学科准教授 宮本圭を中心とする、近畿大学、大阪大学、理化学研究所等の共同研究グループは、多くのマウスの体細胞クローン胚が早期に発生停止する原因として、2つの遺伝子の異常発現が関与していることを世界で初めて発見しました。これらの遺伝子は、通常の受精卵では正常に発現することにより、着床前の胚が問題なく発生しますが、発現が抑制されると胚発生が停止することが明らかになりました。本研究によりクローン胚の低い発生率の一因を遺伝子レベルで解明し、当該遺伝子の発現操作によってクローン胚の発生改善が期待されます。
本件に関する論文が、令和5年(2023年)8月28日(月)23:00(日本時間)に、ライフサイエンスに関する国際的な学術雑誌"Life Science Alliance(ライフ サイエンス アライアンス)"に掲載されました。
【本件のポイント】
●マウスのクローン胚が早期発生停止となる原因遺伝子であるAlyrefとGabpb1を発見
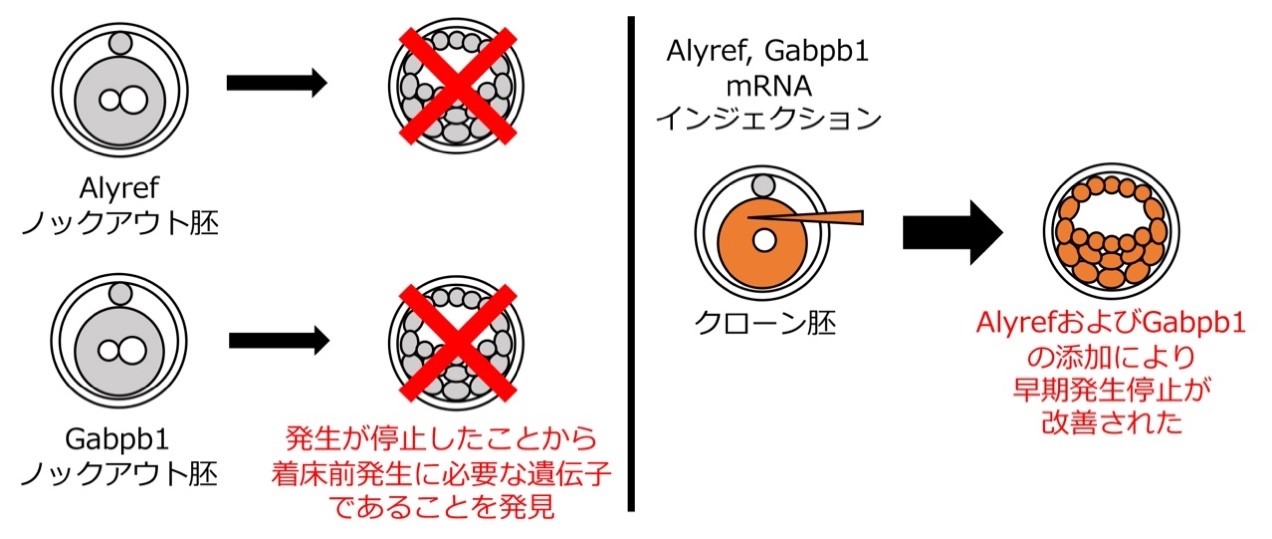
●AlyrefとGabpb1は、着床前の胚発生に必要な遺伝子であり、発現を操作することで、クローン胚早期発生停止が改善することを解明
●本研究成果を用いて、クローン胚の発生率改善に寄与できる可能性に期待
【本件の背景】
体細胞クローン技術※1 は、体細胞核を受精前の卵子に移植して、作製した胚を仮母に移植することにより、ドナー細胞と同じ遺伝情報を持つクローンをつくる技術で、絶滅危惧動物の保全や遺伝子組換え細胞を用いた医療モデル動物の作製など、さまざまな分野での有効利用が期待されています。しかし、多くのクローン胚がごく初期の発生段階で異常を起こすため、クローン個体が誕生する割合(クローン効率)が低いことが問題視されています。特に、胚が着床前発生の段階で停止してしまうと、あらゆる細胞に分化できるES細胞を樹立することができません。
クローン効率が低い原因として、体細胞核が卵子内で初期化※2 される際にさまざまな不具合が生じ、不完全な初期化しか誘導されないことが挙げられます。初期化の不具合を改善し、クローン効率を向上させる研究が世界中で行われ、ヒストン修飾※3 の一つであるヒストンH3の9番目のリジンのトリメチル化(H3K9me3)を核移植後の胚のゲノムから取り除くことにより、クローン効率が大幅に改善することが先行研究で示されました。ここから、クローン胚におけるH3K9me3の異常な蓄積によって重要な胚性遺伝子※4 の活性化が阻害され、発生が停止すると考えられていますが、それに関わる特定の遺伝子はあまりわかっていませんでした
【本件の内容】
研究グループは、クローン胚における着床前胚発生の異常の中でも、特に胚性遺伝子の発現に着目し、クローン胚で受精卵と比較して異常な発現を示す遺伝子を探索しました。その結果、AlyrefとGabpb1という2つの遺伝子を同定しました。これらの遺伝子は、正常な受精卵において胚性遺伝子の大規模な発現が開始する2細胞期に活性化されるはずですが、クローン胚では同時期に発現が低下していることを確認しました。また、ゲノム編集技術※5 を用いて2つの遺伝子の機能を阻害したところ、着床前の早期の段階で受精卵の胚でも発生が停止するとわかりました。
本研究成果により、クローン胚の早期発生停止の原因が遺伝子レベルで明らかになり、将来的に絶滅危惧動物ゲノムの保全や、医療研究用の遺伝子組換え動物の効率的な生産等に貢献することが期待されます。
【論文掲載】
雑誌名:Life Science Alliance(インパクトファクター:5.8@2022)
論文名:
Incomplete activation of Alyref and Gabpb1 leads to preimplantation arrest in cloned mouse embryos
(AlyrefおよびGabpb1遺伝子の不完全な活性化はマウスクローン胚の着床前発生停止へと導く)
著者 :井橋俊哉1†、濱中瑞斗1、加地正弥1、森龍之介1、西崎俊太朗1、森美樹1、今里佑馬1、井上貴美子2,3、的場章悟2,4、越後貫成美2、鷹巣篤志1、中村岬1、松本和也1、安齋政幸5、小倉淳郎2,3、伊川正人6、宮本圭1* *責任著者、†筆頭著者
所属 :1 近畿大学生物理工学部遺伝子工学科、2 理化学研究所バイオリソース研究センター遺伝工学基盤技術室、3 筑波大学大学院生命環境科学研究科、4 東京農工大学共同獣医学科、5 近畿大学先端技術総合研究所、6 大阪大学微生物病研究所
【研究の詳細】
研究グループは、先行研究において、マウスのクローン胚をヒストン脱アセチル化阻害剤であるトリコスタチンA※6(TSA)で処理した後、ビタミンC(VC)添加培地で培養することで、クローン胚におけるH3K9me3の蓄積を低下させ、発生率を大幅に向上させる方法を報告しています。そこで、これまでに同定されているH3K9me3の除去によって発現上昇する遺伝子と、TSAおよびVC処理条件下のクローン胚で発現上昇している遺伝子を比較し、16の遺伝子が共通していることを見出しました。さらに、着床前発生に重要な遺伝子を絞り込むためにsiRNA※7 スクリーニングにより候補遺伝子をそれぞれ発現抑制したところ、AlyrefとGabpb1の2つの遺伝子を、発生に重要な遺伝子として同定しました。
さらに、着床前発生におけるAlyrefとGabpb1の役割を明らかにするため、ゲノム編集技術を用いてAlyrefとGabpb1をノックアウト※8 し、これらの遺伝子の欠損が胚発生に与える影響を調べました。その結果、AlyrefとGabpb1ノックアウトは胚性致死※9 であり、受精胚の発生停止を引き起こしました。また、遺伝子欠損胚をRNA-seq※10 で解析したところ、Alyrefノックアウト胚では多分化能性の維持に必要なNanog遺伝子の発現低下が起こり、将来胎児になる内細胞塊の適切な形成が行われないことがわかりました。また、Gabpb1ノックアウト胚では、ミトコンドリア膜電位※11 の異常やアポトーシス※12 誘導による細胞死が起こり、多くの胚が胚盤胞期までに発生停止することがわかりました。そして、クローン胚でのAlyrefとGabpb1の発現状態を調べたところ、タンパク質レベルで発現が抑制されており、AlyrefとGabpb1のmRNAを細胞に導入して発現を回復させると、クローン胚の着床前発生が促進されました。さらに、AlyrefとGabpb1の発現がクローン胚で抑制されている原因は、H3K9me3によって2つの遺伝子を活性化する転写活性化因子が抑制されている可能性が高いことがわかり、その候補としてKlf16を見つけました。
以上のことから、着床前発生に必要な遺伝子であるAlyrefとGabpb1は、多くのクローン胚では抑制されており、AlyrefとGabpb1の発現抑制状態は、クローン胚低発生の原因の一つであることが明らかになりました。

【今後の展望】
H3K9me3は初期化を阻害する最も重要な因子の一つとして考えられていますが、本研究によって、H3K9me3により初期化が阻害される原因の一つが見つかりました。体細胞におけるH3K9me3の蓄積はiPS細胞の初期化を阻害することも報告されていることから、本研究成果を用いてより効率的な初期化技術の開発が期待されます。
また、クローン技術の一つの障壁となっている、ごく早期での発生停止に関わる遺伝子を発見したことにより、これらの遺伝子の発現を指標として、早期発生停止胚の選別が可能になるかもしれません。さらに、これらの遺伝子の発現を改善させることにより、クローン胚由来ES細胞の効率的な作出も期待され、絶滅危惧動物ゲノムの保全への応用が期待されます。
【研究代表者のコメント】
宮本 圭(みやもと けい)
所属 :近畿大学生物理工学部遺伝子工学科
近畿大学大学院生物理工学研究科
職位 :准教授
学位 :博士(農学)
コメント:クローン胚と受精卵の違いを遺伝子レベルで説明する成果です。本研究により、発生開始して1日程度で既に異常発現を示す重要な遺伝子がわかりました。今後はこれらの遺伝子を指標に、発生能力の高いクローン胚を早期に選別する方法を発展させたいです。また、先行研究で報告されたクローン発生改善法とあわせて、クローン技術を絶滅危惧動物ゲノムの保全などに応用していきたいです。
【用語解説】
※1 体細胞クローン技術:体細胞核を受精前の卵子に移植して(核移植と呼ばれる)、作製した再構築胚の発生を活性化刺激等により誘導し、最終的に再構築クローン胚を仮母に移植することにより、ドナー細胞と同じゲノムを有するクローン動物を作出する技術。
※2 初期化:分化した細胞が、再び体内のすべての細胞に分化できる未分化な状態へと変化する現象。
※3 ヒストン修飾:クロマチンの構成タンパク質であるヒストンに付加される化学修飾。H3K9me3は特に遺伝子発現の抑制に関与する。
※4 胚性遺伝子:受精後まもなく、受精卵(胚)のゲノムから発現する遺伝子。また、これら胚性遺伝子が胚発生の特定の時期に発現する現象を、胚性ゲノム活性化と呼ぶ。
※5 ゲノム編集技術:人工DNA切断酵素によってゲノムDNAにDNA二本鎖切断を誘導し、その修復過程において、標的遺伝子への欠失や変異を導入したり、ドナーコンストラクトを用いた相同組換えによって遺伝子を改変したりする技術。本研究では標的遺伝子の欠失を誘導した。
※6 トリコスタチンA:ヒストン脱アセチル化酵素阻害剤。ヒストン脱アセチル化酵素を阻害する低分子化合物で、培地中に添加することによりヒストンアセチル化状態を高く維持できる。
※7 siRNA:small interfering RNA。20数塩基からなる2本鎖RNAであり、RNA干渉により特異的に遺伝子発現を抑制する。
※8 ノックアウト:遺伝子操作により、特定の遺伝子を欠損(無効化)させること。
※9 胚性致死:発生の段階で分化の異常が生じ、生まれてこないこと。
※10 RNA-seq:次世代シーケンサーを用いて細胞内の遺伝子発現を網羅的に解析する手法。
※11 ミトコンドリア膜電位:細胞小器官であるミトコンドリアの膜内でできた電位差。ミトコンドリアの活性が維持されていることの指標となる。
※12 アポトーシス:細胞の死に方の一種で、プログラムされた細胞死。
【関連リンク】
生物理工学部 遺伝子工学科 准教授 宮本圭(ミヤモトケイ)
https://www.kindai.ac.jp/meikan/1353-miyamoto-kei.html
生物理工学部 遺伝子工学科 教授 松本和也(マツモトカズヤ)
https://www.kindai.ac.jp/meikan/488-matsumoto-kazuya.html
先端技術総合研究所 教授 安齋政幸(アンザイマサユキ)
https://www.kindai.ac.jp/meikan/502-anzai-masayuki.html