膵臓がんの薬が効かなくなるメカニズムを解明 治療が困難となった膵臓がんに対する新たな治療法開発へ

近畿大学医学部(大阪府大阪狭山市)生化学教室主任教授 岡田 斉、近畿大学大学院医学研究科博士課程4年生 スーマン・ダッシュらの研究チームは、膵臓がんの治療に広く使われている抗がん剤「ゲムシタビン(一般名:ゲムシタビン塩酸塩)」が効かなくなる主な原因が、特定の酵素の機能低下にあることを明らかにしました。さらに、ゲムシタビンが効かない膵臓がん細胞では、がん遺伝子MYC※1 の機能と、グルタミンをエネルギー源として利用する能力が高まっており、これらの働きを抑える薬剤が有効であることを明らかにしました。本研究成果は、膵臓がんの標準的治療薬として用いられるゲムシタビンの効果がなくなった症例に対する、新たな治療法の開発につながるものと期待されます。
本件に関する論文が、令和5年(2023年)5月1日(月)に発行される米国癌学会の国際的学術雑誌"Molecular Cancer Research"で特集として紹介されました。
【本件のポイント】
●ゲムシタビンが効かなくなる主な原因が、DNA構成成分であるデオキシシチジンをリン酸化する酵素DCKの機能低下であることを解明
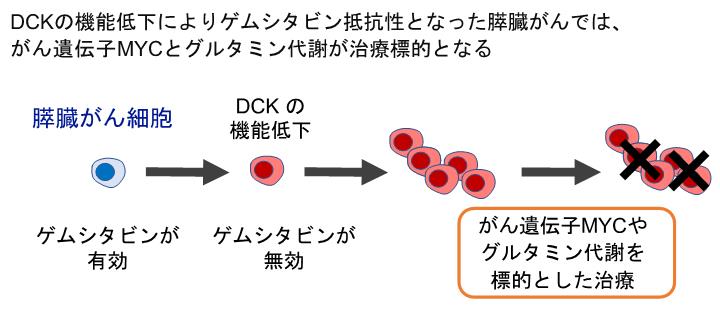
●ゲムシタビンの効果がない膵臓がんでは、がん遺伝子MYCの機能とグルタミン代謝を抑える薬剤が有効となりうることを発見
●ゲムシタビンが効かない膵臓がんの新たな治療法開発につながる研究成果
【本件の背景】
近年、検診や治療法の大幅な改善により、多くの固形がん患者で早期治癒に至るケースが増えています。一方、膵臓がんは、早期発見、早期治療の難しさなどから、過去数十年間にわたり発生率が増加しており、今後もがん死亡の主な原因になると予想されています。
ゲムシタビンは膵臓がんに効果を示す標準的な抗がん剤の一つですが、膵臓がん細胞は、治療経過中にしばしば抗がん剤耐性を獲得し、治療効果が認められなくなることが臨床上の課題となっています。ゲムシタビンが無効となった膵臓がんは治療の選択肢が限られていることから、抗がん剤が効かなくなる機序の解明、耐性の克服および新たな治療法の開発が求められています。
【本件の内容】
研究チームは、ゲノム編集※2 という手法を用いて、膵臓がん細胞株※3 で約2万個のヒトの遺伝子を個別に破壊し、ゲムシタビン抵抗性の原因となる遺伝子の探索を行いました。その結果、DNAの構成成分であるデオキシシチジンをリン酸化する酵素DCK(Deoxycytidine kinase)の機能低下が、ゲムシタビンが効かなくなる主原因の一つであることを見出しました。
また、DCKの機能低下が、がん遺伝子MYCの機能と、アミノ酸の一つであるグルタミンをエネルギー源として利用する能力を高めることを発見しました。さらに、これらの機能を抑える働きをもつ薬剤(MYC阻害剤、グルタミンアナログ)が、ゲムシタビンの効かなくなったがん細胞に実際に有効であることを明らかにしました。
本研究成果は、膵臓がんの標準的治療薬として用いられるゲムシタビンの効果がなくなった症例に対する、新たな治療法の開発につながるものと期待されます。
【論文概要】
掲載誌:Molecular Cancer Research(インパクトファクター:6.333@2022)
論文名:MYC/Glutamine Dependency Is a Therapeutic Vulnerability in Pancreatic Cancer with Deoxycytidine Kinase Inactivation-Induced Gemcitabine Resistance
(DCKの不活性化によりゲムシタビン抵抗性となった膵臓がんでは、がん遺伝子MYCとグルタミン代謝が治療標的となる)
著者 :Suman Dash 1,2、上田 健 1,2、古室 暁義 1、天野 恭志 1、本多 賢彦 1、河津 正人 3、岡田 斉 1,2,4※ ※ 責任著者
所属 :1 近畿大学医学部生化学教室、2近畿大学大学院医学研究科、3 千葉県がんセンター、4 近畿大学アンチエイジングセンター
【研究詳細】
研究チームは、膵臓がん細胞株のうち、ゲムシタビンによって容易に細胞死が誘導される細胞株を選び、ゲノム編集という手法を用いて、約2万個のヒトの遺伝子を個別に破壊しました。遺伝子破壊によってゲムシタビンが存在していても増殖を続けることができるようになった細胞を利用して、ゲムシタビン抵抗性の原因となる遺伝子のスクリーニングを行いました。その結果、DNAの構成成分であるデオキシシチジンをリン酸化する酵素DCKの機能低下が、ゲムシタビン抵抗性の主原因の一つであることを見出しました。
さらに、研究チームは、DCK遺伝子を破壊して作成したゲムシタビン抵抗性膵臓がん細胞株と、既報のDCK遺伝子の発現が低い膵臓がん症例の遺伝子発現データを比較解析し、DCKの機能低下は、がん遺伝子MYCの機能と、アミノ酸の一つであるグルタミンをエネルギー源として利用する能力を高めることを見出しました。また実際に、これらの機能を抑える働きをもつ薬剤(MYC阻害剤、グルタミンアナログ)が、DCK遺伝子を破壊したゲムシタビン抵抗性細胞に細胞死を誘導できることを明らかにしました。
本研究成果は、膵臓がんの標準的治療薬であるゲムシタビンに抵抗性を生じるメカニズムおよび、がん遺伝子MYCやグルタミン代謝が、ゲムシタビン抵抗性膵臓がんに対する有望な治療標的となる可能性を報告するものです。
【研究代表者コメント】
岡田 斉(おかだ ひとし)
所属 :近畿大医学部生化学教室
職位 :主任教授
学位 :医学博士
コメント:本研究では、遺伝子破壊により樹立したゲムシタビン抵抗性膵がん細胞を用いて、薬剤耐性機序を明らかにし、その結果、耐性細胞の新規治療標的を見出しました。今後、今回の成果を発展させ、がんの個別化医療に貢献できればと思います。
【用語解説】
※1 がん遺伝子MYC:さまざまな組織のがん化に関わることが知られる代表的な遺伝子の一つ。
※2 ゲノム編集:生物の遺伝情報であるDNAの配列を書き換えることができる技術。令和2年(2020年)、本技術に関連する手法を開発したドイツの研究機関とアメリカの大学の研究者2人がノーベル化学賞に選ばれた。
※3 がん細胞株:がん組織から得られた細胞を、長期間実験室などで適切な栄養素を含む培養液を用いて培養することにより、安定した性質を示すようになった細胞を指す。がん細胞の特性を調べる目的で利用される。
【関連リンク】
医学部 医学科 教授 岡田 斉(オカダ ヒトシ)
https://www.kindai.ac.jp/meikan/1297-okada-hitoshi.html