難治性の肝細胞がんに対して世界初の画期的な根治治療法を開発 肝細胞がんの標準治療確立へ道筋
近畿大学医学部(大阪府大阪狭山市)内科学教室(消化器内科部門)主任教授工藤正俊らの研究グループは、これまで治療法が存在しなかった多発・大型肝がんのなかでも特に進行した肝がん患者に対して分子標的薬※1 レンバチニブ(エーザイ)を先行投与した後に肝動脈塞栓療法(TACE)※2 を追加するという新規治療法(LEN-TACE sequential 治療)を考案し、1970年代に確立された標準治療法TACEと比較して生存期間を約2倍近く延長させることを世界で初めて証明しました。また、この中の20%弱の患者の体内から肝がんが全て消失し、完全に治癒し現在も無治療のまま経過している人もいるという極めて治療効果の高い方法であることを報告しました。この臨床研究は平成20年(2008年)から平成30年(2018年)の期間に国内7施設と香港の1施設の計8施設(詳細は後述)の多施設共同臨床研究として実施されたものです。この成果が発表されることにより、いわば世界の医療が変わるということになり、これまで標準治療が存在しなかった領域における世界初の画期的な治療法の開発と位置付けられます。
本件に関する論文が、令和元年(2019年)7月31日(水)17:00(日本時間)、腫瘍学分野の専門誌である"Cancers"にオンライン掲載されました。
【本件のポイント】
●標準治療が無かった全肝多発・大型肝がんの根治的になりえる治療法を確立
●進行した肝がんに対しレンバチニブ先行TACE治療にて生存期間を延長することが明らかに
●難治がんステージの肝がんに対して、新たな標準治療へ位置づけ
【本件の内容】
肝細胞がんは日本人のがん死亡原因の第5位を占め現在でも毎年約2万8千人の方が亡くなられている難治がんの一つです。肝細胞がんのステージには(1)早期肝がん(3cm以下、3個以下)(2)少数多発・中型肝がん(中等度早期)、(3)全肝多発・大型肝がん(中等度進行期)(4)進行肝がん(脈管浸潤、遠隔転移あり)(5)末期肝がんの大きく5期に分類されます。(1)の早期肝がんには切除やラジオ波が治療法として確立されており(2)の少数多発・中型肝がん(早期)にはTACEが標準治療として確立されています。また(4)の脈管浸潤や遠隔転移を伴った進行肝がんに対しては分子標的薬が標準治療法として確立されており、免疫チェックポイント阻害剤※3 も治験がさかんに行われています。しかしながら患者数が最も多い(3)の全肝多発・大型肝がん(進行期)に対しては、1970年代に開発された標準治療であるTACEの効果が乏しく再発が繰り返しおこり、進行がんや末期がんに移行する、とされている重要なステージにもかかわらず、このステージの肝がんに対しては標準治療が確立されていませんでした。従ってこのステージの肝がんに対する治療法の開発は世界中の肝がん治療医にとって急務の課題であり、長い間最大のテーマでありましたが、現在に至るまで未解決の分野となっていました。
本研究では通常、進行肝がんに対してのみ使用する分子標的薬レンバチニブをこのステージの肝がんに対して最初の導入治療法として使用することにより(1)腫瘍の縮小・壊死効果を誘導(2)腫瘍の血管は太かったり細かったりといびつですがその血管径を正常の血管サイズに戻す作用(3)後から追加する抗がん剤や塞栓物質を腫瘍内に均一に分布させる作用(4)分子標的薬の最大効果の出ているタイミングでTACEを加えることで、TACE後に誘導される血管新生因子(腫瘍の増殖・浸潤転移を引き起こす作用を持つ因子)を抑制する作用により再発・転移を防げるのではないか、という仮説を立証しました。
そして、分子標的薬レンバチニブをこのステージの肝がんの患者さんに投与し、その後TACEを加えるというLEN-TACE sequential治療によりTACE単独で治療を行うより、約2倍近く全生存期間を延長させることを証明しました。また、死亡リスクとしては約52%下げることが判明しました(ハザード比※4 0.48, p<0.01)。
この新しい治療法は生存延長効果を証明したことにより世界の肝がんの治療体系を大きく変え、新しい標準治療法として位置づけられることが予測されています。
【論文掲載】
論 文 名:Lenvatinib as an Initial Treatment in Patients with Intermediate-stage Hepatocellular Carcinoma Beyond up-to-seven Criteria and Child-Pugh A Liver Function:A Proof-of-Concept Study
掲 載 誌:Cancers(IF:6.162)
共筆頭著者:*工藤 正俊1)、上嶋 一臣1)、Stephan Chan2)、南 知宏1)、千品 寛和1)、青木 智子1)、田北 雅弘1)、萩原 智1)、南 康範1)、依田 広1)、竹中 完1)、櫻井 俊治1)、渡邊 智裕1)、盛田 雅弘3)、小川 力3)、和田 幸之4)、池田 公史5)、石井 浩6)7)、泉 並木8)、西田 直生志1)
*責任著者
1)近畿大学医学部内科学教室(消化器内科部門)、2)Translational Oncology, The Chinese University of Hong Kong、3)高松赤十字病院消化器内科、4)国立病院機構九州医療センター肝胆膵外科、5)国立がん研究センター東病院肝胆膵内科、6)がん研有明病院消化器内科、7)千葉県がんセンター臨床研究センター、8)武蔵野赤十字病院消化器内科
【研究詳細】
分子標的薬レンバチニブは、それまでの唯一の進行肝がんに対する標準治療薬であったソラフェニブに対して、平成29年(2017年)に過去10年間で初めてソラフェニブに対して生存延長効果が非劣勢であることを示した唯一の分子標的薬であります。その臨床試験結果の詳細は平成30年(2018年)のLancetに掲載されました(Kudo M, et al. Lancet 2018)。この薬剤は現在、アジアはもちろんのこと北米、南米、欧州など全世界で承認され進行肝がん患者さんの第一選択の治療薬として現在積極的に使用されています。またレンバチニブは進行肝がんに対して生存延長効果を示しただけでなく腫瘍縮小・壊死効果にも優れ奏効率※5 は40.6%と極めて抗腫瘍効果に優れることが示されました。一方、進行肝がんになる手前の脈管浸潤・遠隔転移のない多発・大型肝がんの進行期に対する標準治療はかつての標準治療であったTACEの効果が悪く、TACEを行っても再発の繰り返しで肝機能を悪くして死亡時期を早め進行がん、末期がんに移行していく症例が多く見られました。このステージは全世界において治療に難渋する病態であり、いわば標準治療の存在しない未開の難治がんであるといえます。
工藤らの研究チームはこのレンバチニブの腫瘍縮小・壊死効果が高いことに着目し、脈管浸潤や遠隔転移のない進行がんになる前の多発・大型肝がんのステージから敢えてTACEを行わずにレンバチニブを先行投与してからTACEを行うこと(LEN-TACE sequential治療)がTACEの効果を高めるのではないか、との仮説を立てました。このような仮説を持つ研究者は当時世界中に殆どいませんでした。研究チームはその仮説の検証のため、平成20年(2008年)から平成30年(2018年)の期間、このステージの患者に初回治療としてレンバチニブを投与した37例を解析しました。方法は同時期にTACEを施行した患者139例と治療効果についての比較検討を行いました。また患者背景を均一にする統計手法である傾向スコアマッチング(propensity score matching)※6 を用いた結果、30例のレンバチニブ投与先行TACE群と60例のTACE単独治療群を抽出し、奏効率(ORR)、肝機能悪化の推移(ALBI score)※7、無増悪生存期間(PFS)※8、生存期間(OS)※9 について比較検討を行いました。
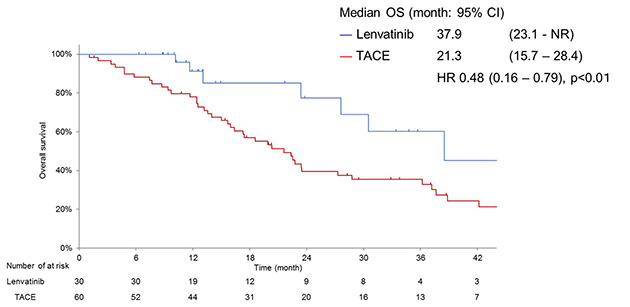
その結果レンバチニブ先行投与群の奏効率は73.3%とTACE単独群の奏効率33.3%と比較して驚異的に高く(Odds ratio 5.29, p<0.001)、肝機能の悪化も有意に低く(p<0.01)、またPFSも劇的にレンバチニブ先行群が優っていました(16.0か月対3.0か月、ハザード比 0.19, p<0.001)。結果として最大の効果指標としてのOS延長効果はレンバチニブ先行群37.9か月に対しTACE単独治療群21.3か月でありました(ハザード比 0.48, p<0.01)。またレンバチニブ先行群の中には4例が完全奏効を示し、がん細胞が全て消失して治癒し現在、全く無治療で元気に経過観察している患者も出現しています。従ってこの治療法はある程度進行した多発・大型肝がんでも完全治癒も期待できる画期的治療法と位置付けられます。
この成果が発表されることによりいわば世界の医療が変わる、ということになりこれまで標準治療が存在しなかった領域における世界初の画期的な治療法の開発と位置付けられます。
【用語解説】
※1 分子標的薬
正常の細胞も障害を受ける従来の抗がん剤とは異なり、がん細胞の増殖などに関わる特定の分子のみを狙い撃ちして、その働きを抑える薬です。肝がんの場合はレンバチニブ(レンビマ)の他にソラフェニブ(ネクサバール)、レゴラフェニブ(スチバーガー)、ラムシルマブ(サイラムザ)など4種類の薬が承認されています。
※2 肝動脈塞栓療法(TACE)
肝臓は肝動脈と門脈という2つの血管から栄養されています。肝臓がんは肝動脈のみから100%酸素と栄養を受けているため、カテーテルを通して肝動脈を完全に塞いで兵糧詰めにすることにより、がん細胞のみを死滅させる方法です。腫瘍のサイズや個数が少ない場合は、この方法は効果的ですがサイズが大きい場合や個数が多い場合はカテーテルを腫瘍の近くまで近づけることが難しくなり効果も悪くなるばかりか正常な周りの肝組織の細胞もある程度死滅してしまうので肝機能を悪くさせるのが欠点です。
※3 免疫チェックポイント阻害剤
本来生体にはがんが発生するとリンパ球が活性化され、がん細胞を攻撃して排除しようとしますが、その反応が起こると、がん細胞はPD-L1という分子を出してリンパ球の表面のPD-1分子と結合することによりがん細胞からの攻撃から逃れるようになり、どんどん増殖して浸潤・転移します。これに対してPD-1分子やPD-L1分子に結合する抗体を投与するとこのがん細胞の免疫から逃れる仕組みがブロックされ再びリンパ球ががん細胞を攻撃するようになります。この仕組みを発見したのが京都大学の本庶 佑教授で平成30年(2018年)のノーベル賞(医学・生理学分野)を受賞しました。
※4 ハザード比
ハザード比とは統計学上の用語で、臨床試験などで使用する相対的な危険度を客観的に比較する方法です。英語でHazard Ratio、略してHRとも言います。
ある臨床試験で検討したい新治療法Aと比較対象の標準治療法Bとを比べたとき、ハザード比が1であれば2つの治療法に差はなく、ハザード比が1より小さい場合には治療Aの方が有効と判定され、その数値が小さいほど有効であるとされます。例えばA薬と対象のB薬を比較するというある臨床試験でハザード比が0.94という結果であれば、A薬はB薬よりリスクを6%減少させたという意味になります。今回の臨床試験のOSのハザード比は0.48ですので今回の新しい治療法がかなり良好に死亡リスクを下げる、と言えます。
※5 奏効率 ORR(Objective Response Rate)
抗がん剤の治療成績の評価に一般的に用いられる指標であり、治療前の腫瘍サイズに比べ、最大の腫瘍縮小効果(もしくは腫瘍壊死効果)が100%(腫瘍の完全消失もしくは完全壊死)の場合を完全奏効(complete response: CR)と呼び、30%以上の腫瘍縮小効果(もしくは腫瘍壊死効果)が得られた場合を部分奏効(partial response: PR)と呼びます。奏効率とは全体集団の中でのCR+PRの症例の割合を表す言葉であり、高ければ高いほど抗腫瘍効果が強いとされています。
※6 傾向スコアマッチング(propensity score matching)
臨床的有用性を証明する統計手法の一つ。最も重要な問題(例えば、ある治療法が標準治療に対して優ること)の証明のためには前向きの無作為化割り付け臨床試験(RCT)が最もエビデンスレベルの高い方法です。しかし次にエビデンスレベルの高い方法として昭和58年(1983年)に確立されたのがこの手法です。すなわち、生存に関連する背景因子を両群に均一にすることにより、いわゆる「選択バイアスを排除する手法」として近年、推奨されている統計解析手法です。
※7 肝機能悪化の推移(ALBI score)
従来は肝予備能の指標としてはChild-Pugh分類やChild-Pughスコアが用いられてきましたが、Child-Pugh分類よりも正確かつ客観的な指標としてアルブミンとビリルビンの2つの項目から計算される指標です。最近はChild-PughスコアよりもALBIスコアの方が用いられることが多くなりました。日本肝癌研究会の取扱い規約にも採用されています。計算式は複雑ですが多くの病院では中央検査室での自動計算結果が電子カルテに表示されるので使用は極めて容易です。
※8 無増悪生存期間 PFS(progression-free survival)
抗がん剤の治療成績の評価に一般的に用いられる指標であり、試験登録日もしくは治療開始日から病勢増悪もしくは死亡が確認されるまでの期間と定義されます。中央値を代表値として表現することが多い。
※9 全生存期間 OS(Overall Survival)
抗がん剤の治療成績の評価に一般的に用いられる指標。対象となる患者さんの試験登録日もしくは治療開始日から死亡が確認されるまでの期間と定義される。中央値を代表値として表現することが多い。
【関連リンク】
医学部医学科 教授 工藤 正俊(クドウ マサトシ)
https://www.kindai.ac.jp/meikan/569-kudou-masatoshi.html
医学部医学科 医学部講師 上嶋 一臣(ウエシマ カズオミ)
https://www.kindai.ac.jp/meikan/1540-ueshima-kazuomi.html
医学部医学科 医学部講師 田北 雅弘(タキタ マサヒロ)
https://www.kindai.ac.jp/meikan/1772-takita-masahiro.html
医学部医学科 医学部講師 萩原 智(ハギハラ サトル)
https://www.kindai.ac.jp/meikan/1577-hagihara-satoru.html
医学部医学科 医学部講師 南 康範(ミナミ ヤスノリ)
https://www.kindai.ac.jp/meikan/1525-minami-yasunori.html
医学部医学科 医学部講師 依田 広(イダ ヒロシ)
https://www.kindai.ac.jp/meikan/1980-ida-hiroshi.html
医学部医学科 医学部講師 竹中 完(タケナカ マモル)
https://www.kindai.ac.jp/meikan/2247-takenaka-mamoru.html
医学部医学科 医学部講師 櫻井 俊治(サクライ トシハル)
https://www.kindai.ac.jp/meikan/1675-sakurai-toshiharu.html
医学部医学科 准教授 渡邉 智裕(ワタナベ トモヒロ)
https://www.kindai.ac.jp/meikan/1505-watanabe-tomohiro.html
医学部医学科 准教授 西田 直生志(ニシダ ナオシ)
https://www.kindai.ac.jp/meikan/653-nishida-naoshi.html