ペプチド医薬品の鍵を握る酵素を制御することに成功 薬剤耐性菌に対応する新薬研究開発への応用に期待
近畿大学薬学部(大阪府東大阪市)講師 石川文洋を中心とする研究グループは、アミノ酸の結合体であるペプチドの特性を決定する酵素「アデニル化酵素」を改良し、自然界に存在しない物質もペプチドの特性とできる可能性がある人工アデニル化酵素を開発しました。
本研究成果により、安価で副作用が少ない次世代の医薬品と言われ、抗菌薬やがんなどの治療薬としてすでに実用化されている「ペプチド医薬品」において、研究開発のスピード向上や、医薬品に耐性を持つ薬剤耐性菌への対応薬の開発が容易になる可能性が見込まれ、今後のペプチド医薬品開発に大きく貢献することが期待されます。
本件に関する論文が、平成31年(2019年)4月4日(木)19:00(日本時間)に、化学分野における総合学術誌の中心的雑誌、ドイツ化学会誌「Angewandte Chemie International Edition」にオンライン掲載されました。
【本件のポイント】
●困難とされていたアデニル化酵素を人為的に改良し、酵素の潜在能⼒を見出した
●自然界には存在しない物質も許容し、様々な特性を持つペプチドの開発が可能に
●次世代の医薬品であるペプチド医薬品の研究開発の進展に貢献
【本件の内容】
近年、従来使われてきた医薬品に耐性を持つ薬剤耐性菌が増加する一方、それに対する医薬品の開発がなかなか進まない状況が課題となっています。薬剤開発の原料の半分以上は自然界に存在する微生物や植物などの生物由来の天然物質です。その一つであるペプチドは、神経伝達物質等の生理活性物質※1 として人間の体内でも働いていることから、ペプチドを原料としたペプチド医薬品は安全性の高さに注目が集まっています。
ペプチド系の天然物が薬品としてどのような特性を持つかを決定するのが、アデニル化酵素です。そのため、アデニル化酵素を制御することによって、様々な特性を持つペプチドを開発し、医薬品開発に活用しようと研究されてきましたが、汎用性の高い有効な方法は未だ開発されていませんでした。酵素と結びつくことでペプチドの特性を決定づける物質「基質」と酵素は鍵と鍵穴の関係に例えられるほど厳密であり、自由に酵素と基質を組み合わせることができなかったためです。
今回、アデニル化酵素を改良し、基質と結びつく部位を拡張したところ、様々な基質と結びつく酵素へ変貌しました。しかも、天然由来の物質だけでなく、人工物とも結びつくことを確認し、新たな特性をペプチドに持たせられる可能性が生まれました。
本研究成果により、ペプチド医薬品の開発研究が加速し、新薬の創出率の向上が期待されます。
【掲載誌について】
雑誌名 :"Angewandte Chemie International Edition"化学分野における総合学術誌の中心的雑誌であり、Wiley-VCHが発行するドイツ化学会誌(インパクトファクター:12.102)
論文名 :An engineered aryl acid adenylation domain with a capacious active site microenvironment(アデニル化酵素の新しい改良法)
著 者:Fumihiro Ishikawa(近畿大学薬学部講師), Akimasa Miyanaga(東京工業大学理学研究院化学系助教), Hinano Kitayama(近畿大学薬学部医療薬学科5年生), Shinya Nakamura(近畿大学薬学部講師), Isao Nakanishi(近畿大学薬学部教授), Fumitaka Kudo(東京工業大学理学研究院化学系准教授), Tadashi Eguchi(東京工業大学理学研究院化学系教授),Genzoh Tanabe(近畿大学薬学部教授)
筆頭著者:Fumihiro Ishikawa 石川文洋, Akimasa iyanaga 宮永顕正
責任著者:Fumihiro Ishikawa 石川文洋
【研究の詳細】
微生物が産生する非リボソームペプチド※2(抗生物質バンコマイシン、抗腫瘍性ブレオマイシンA2、免疫抑制剤シクロスポリンAなど)は、多様な化学構造および有用な生理活性を有することから、創薬シーズとして有用です。実際、数多くの非リボソームペプチドが医薬品として使用されています。また、その化学構造の複雑さから、酵素的に多様な類縁体を創製する手法の確立が待たれています。
非リボソームペプチドは、非リボソームペプチド合成酵素(NRPS)※3 によって生合成されます。NRPSのアデニル化酵素は、アミノ酸や芳香族カルボン酸などを非リボソームペプチドへ導入する働きを持っています。すなわち、アデニル化酵素は非リボソームペプチド生合成において、基質を選択する非常に重要な役割を担っているということです。そのため、アデニル化酵素の基質特異性※4 を変換する試みが数多く報告されていますが、その厳密さゆえ、汎用性の高い方法は存在しませんでした。
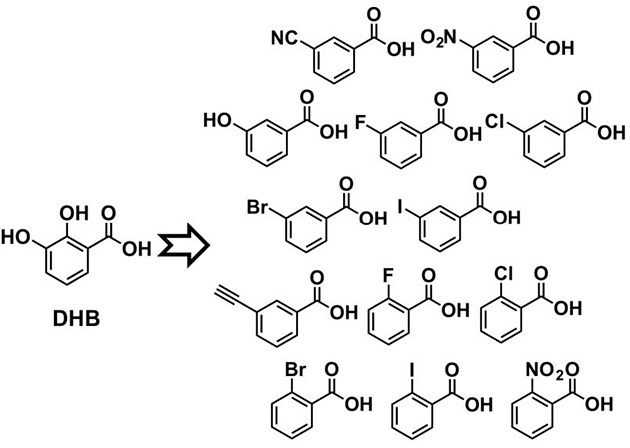
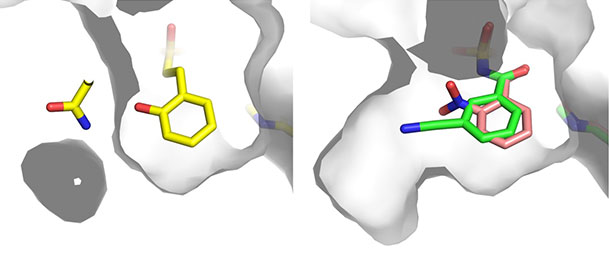
石川らの研究グループは、2,3-ジヒドロキシ安息香酸(DHB)を基質とするアデニル化酵素(EntE)をモデルに基質特異性の拡張を検討しました。まず、EntEの構造情報に基づき機能改変を行い、自然界には存在しないさまざまな基質を許容する人工アデニル化酵素を開発しました(図1)。さらに、そのX線結晶構造解析※5 により、基質特異性拡張の分子基盤を明らかにしました(図2)。改良されたアデニル化酵素の基質結合部位は、ベンゼン環を共通の認識部位としさまざまな官能基を許容する非常に大きな空間を有していることがわかりました。
なお本研究は、文部科学省科学研究費補助金・新学術領域研究(研究領域提案型)「生物合成系の再設計による複雑骨格機能分子の革新的創成科学」の支援のもと行われました。
【用語解説】
※1 生理活性物質:
生体内のさまざまな生命活動を調節したり、影響を与えたりする物質の総称。
※2 非リボソームペプチド:
微生物が産生するペプチドの中で、リボソームを経由せずに合成されるペプチド。抗生物質バンコマイシン、抗腫瘍性ブレオマイシンA2、免疫抑制剤シクロスポリンAだけでなく、抗生物質ダプトマイシン、抗生物質ポリミキシンB、抗腫瘍性アクチノマイシンDなどその多くが医薬品として使用されている。
※3 非リボソームペプチド合成酵素:
非リボソームペプチドを合成する酵素(タンパク質)。
※4 基質特異性:
基質と酵素は"鍵"と"鍵穴"の関係に例えられる。そのため特定の基質にしか作用しない。よく似た構造を持つものでも基質とならない場合が多い。この特定の基質にのみ限定的に働く基質の選択性を基質特異性と呼ぶ。
※5 X線結晶構造解析:
タンパク質の立体構造を決定する手法。タンパク質が機能する詳細なメカニズムを知ることができる。
【関連リンク】
薬学部医療薬学科 講師 石川 文洋(イシカワ フミヒロ)
https://www.kindai.ac.jp/meikan/2073-ishikawa-fumihiro.html
薬学部創薬科学科 講師 中村 真也(ナカムラ シンヤ)
https://www.kindai.ac.jp/meikan/381-nakamura-shinya.html
薬学部医療薬学科 教授 田邉 元三(タナベ ゲンゾウ)
https://www.kindai.ac.jp/meikan/354-tanabe-genzou.html